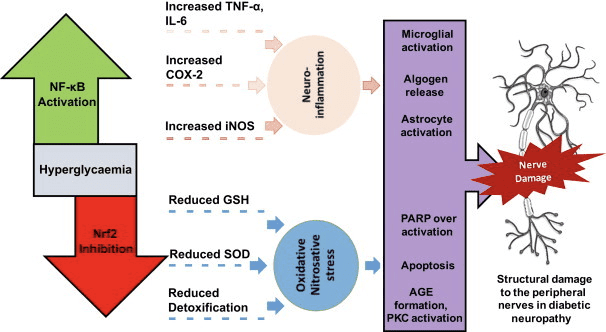
Daugiafunkciai ketoninių kūnų vaidmenys
Ketoninius kūnus sukuria kepenys ir jie naudojami kaip energijos šaltinis, kai gliukozės nėra lengvai prieinama žmogaus organizme. Du pagrindiniai ketoniniai kūnai yra acetoacetatas (AcAc) ir 3-beta-hidroksibutiratas (3HB), o acetonas yra trečias ir mažiausiai gausus ketono kūnas. Ketonų kraujyje visada yra, o nevalgius ir ilgai mankštinantis jų koncentracija padidėjaKetogenezę yra biocheminis procesas, kurio metu organizmai gamina ketoninius kūnus per riebalų rūgščių ir ketogeninių amino rūgščių skilimą.
Ketoniniai kūnai daugiausia generuojami kepenų ląstelių mitochondrijos. Ketogenezė atsiranda, kai kraujyje yra mažai gliukozės kiekio, ypač po to, kai išlieka kitų ląstelinių angliavandenių atsargų, tokių kaip glikogenas. Šis mechanizmas taip pat gali atsirasti, kai insulino nepakanka. Galų gale ketoninių kūnų gamyba inicijuojama, siekiant pagaminti energijos, kuri žmogaus organizme laikoma riebalų rūgštimis. Ketogenezė pasireiškia mitochondrijose, kur jis nepriklausomai reguliuojamas.
Abstraktus
Ketonų kūno metabolizmas yra pagrindinis fiziologinės homeostazės mazgas. Šioje apžvalgoje aptariama, kaip ketonai atlieka atskirus tiksliai reguliuojančius medžiagų apykaitos procesus, kurie optimizuoja organų ir organizmo savybes esant skirtingoms maistinių medžiagų liekanoms ir apsaugo nuo uždegimo ir sužeidimų daugelio organų sistemose. Tradiciškai vertinama kaip medžiagų apykaitos substratai, įtraukti į angliavandenių ribojimą, pastarieji pastebimai pabrėžia ketoninių kūnų kaip svarbių medžiagų apykaitos ir signalizacijos tarpininkų svarbą, kai yra daug angliavandenių. Kuriant kepenų kūnų vėžio numatomus vaidmenis papildant repertuarą žinomų terapinių variantų, susijusių su nervų sistemos ligomis, atsirado intriguojantys apsauginiai vaidmenys širdyje ir kepenyse, atidarant terapines galimybes nutukimo ir širdies bei kraujagyslių ligoms. Aptariami ketonų metabolizmo ir signalizacijos ginčai, siekiant suderinti klasikinę dogmą su šiuolaikiniais stebėjimais.
Įvadas
Ketoniniai kūnai yra gyvybiškai svarbus alternatyvus metabolinis kuro šaltinis visoms gyvenimo sritims, eukarioms, bakterijoms ir archėjoms (Aneja et al., 2002; Cahill GF Jr, 2006; Krishnakumar et al., 2008). Ketoninis organizmo metabolizmas organizme skatina smegenis epizodiniais maisto medžiagų trūkumo laikotarpiais. Ketonų kūnai yra susipynę su svarbiais žinduolių metabolizmo keliais, tokiais kaip a-oksidacija (FAO), trikarboksirūgšties ciklas (TCA), gliukoneogenezė, de novo lipogenezė (DNL) ir sterolių biosintezė. Žinduolių ketoniniai kūnai daugiausia gaminami kepenyse iš FAO gauto acetil-CoA, ir jie pernešami į ekstepepatinius audinius galutinei oksidacijai. Ši fiziologija suteikia alternatyvų kurą, kurį papildo santykinai trumpas badavimo laikotarpis, kuris padidina riebalų rūgščių prieinamumą ir sumažina angliavandenių prieinamumą (Cahill GF Jr, 2006; McGarry ir Foster, 1980; Robinson ir Williamson, 1980). Ketonų kūno oksidacija tampa reikšmingu indėliu į bendrą žinduolių energijos apykaitą ekstrahepatiniuose audiniuose daugybėje fiziologinių būsenų, įskaitant nevalgymą, badavimą, naujagimių periodą, po mankštos, nėštumą ir mažai angliavandenių turinčių dietų laikymąsi. Cirkuliuojančios bendros ketonų kūno koncentracijos sveikiems suaugusiesiems žmonėms paros cirkuliacija paprastai būna maždaug 100–250 µM, po ilgo fizinio krūvio arba 1 valandų nevalgius padidėja iki ~ 24 mM, o patologinėse būsenose, tokiose kaip diabetinė ketoacidozė, gali kauptis iki 20 mM ( Cahill GF Jr, 2006; Johnson ir kt., 1969b; Koeslag ir kt., 1980; Robinson ir Williamson, 1980; Wildenhoff ir kt., 1974). Žmogaus kepenys per dieną gamina iki 300 g ketoninių kūnų (Balasse ir Fery, 1989), kurie sudaro 5–20% visų energijos sąnaudų maitinant, nevalgius ir badaujant (Balasse ir kt., 1978; Cox et. al., 2016).
Naujausi tyrimai dabar pabrėžia būtiną vaidmenį ketoninių organizmų žinduolių ląstelių metabolizmui, homeostazei ir signalizavimui esant įvairiems fiziologiniams ir patologiniams būklėms. Be energetinių deguonies tiekimo ekstrahepaziniuose audiniuose, pavyzdžiui, smegenyse, širdyje ar skeleto raumenyse, ketonų kūnai atlieka svarbiausius vaidmenis kaip signalizavimo tarpininkai, baltymo post-transliacijos modifikacijos (PTM) varikliai ir uždegimo bei oksidacinio streso moduliatoriai. Šioje apžvalgoje pateikiami tiek klasikiniai, tiek modernūs ketoninių kūnų pleiotropinių vaidmenų ir jų metabolizmo požiūriai.
Ketonų kūno metabolizmo apžvalga
Kepenų ketogenezės greitį reguliuoja organizuota riebalų fiziologinių ir biocheminių transformacijų serija. Pirminiai reguliatoriai yra riebalų rūgščių lipolizė iš triacilglicerolių, pernešimas į hepatocitų plazmos membraną ir per ją, pernešimas į mitochondrijas per karnitino palmitoiltransferazę 1 (CPT1), a-oksidacijos spiralė, TCA ciklo aktyvumas ir tarpinės koncentracijos, redokso potencialas ir hormoniniai reguliatoriai. šių procesų, daugiausia gliukagonas ir insulinas [apžvelgta (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferre et al., 1983; Kahn et al., 2005; McGarry and Foster (1980; Williamson ir kt., 1969)]. Klasikiniu požiūriu ketogenezė vertinama kaip išsiliejimo kelias, kuriame a-oksidacijos būdu gautas acetil-CoA viršija citrato sintazės aktyvumą ir (arba) oksaloacetato prieinamumą kondensacijai formuoti citratą. Trijų anglies tarpiniai produktai pasižymi antiketogeniniu aktyvumu, tikriausiai dėl jų gebėjimo išplėsti oksaloacetato telkinį vartojant acetil-CoA, tačiau vien kepenų acetil-CoA koncentracija ketogeninio kiekio nenustato (Foster, 1967; Rawat ir Menahan, 1975; Williamson ir kt., 1969). Ketogenezės reguliavimas hormoniniais, transkripcijos ir posttransliaciniais įvykiais kartu patvirtina mintį, kad molekuliniai mechanizmai, kurie sureguliuoja ketogeninį greitį, lieka iki galo nesuprantami (žr. HMGCS2 ir SCOT / OXCT1 reglamentą).
Ketogenezė pirmiausia pasireiškia kepenų mitochondrijų matricoje greičiu, proporcingu bendram riebalų oksidavimui. Pervežus acilo grandinėms per mitochondrijų membranas ir a-oksidavus, 3-hidroksimetilglutaril-CoA sintazės (HMGCS2) mitochondrijų izoforma katalizuoja likimą, įpareigojant kondensuoti acetoacetil-CoA (AcAc-CoA) ir acetil-CoA, kad susidarytų HMG-CoA (1A pav.). HMG-CoA liazė (HMGCL) skaldo HMG-CoA, kad išsiskirtų acetil-CoA ir acetoacetatas (AcAc), o fosfatidilcholinui priklausoma mitochondrijų d-OHOH dehidrogenazė pastaruosius paverčia d-a-hidroksibutiratu (d-OHOH) ( BDH1) NAD + / NADH susietoje beveik pusiausvyros reakcijoje (Bock ir Fleischer, 1975; LEHNINGER ir kt., 1960). BDH1 pusiausvyros konstanta palanki d-? OHB gamybai, tačiau AcAc / d-? OHB ketoninių kūnų santykis yra tiesiogiai proporcingas mitochondrijų NAD + / NADH santykiui, taigi BDH1 oksidoreduktazės aktyvumas moduliuoja mitochondrijų redokso potencialą (Krebs ir kt., 1969; Williamson ir kt., 1967). AcAc taip pat gali spontaniškai dekarboksilinti iki acetono (Pedersen, 1929), saldaus kvapo šaltinio žmonėms, kenčiantiems nuo ketoacidozės (ty, bendri serumo ketoniniai kūnai> ~ 7 mM; AcAc pKa 3.6,? OHB pKa 4.7). Mechanizmai, per kuriuos ketoniniai kūnai gabenami per mitochondrijų vidinę membraną, nėra žinomi, tačiau AcAc / d-? OHB iš ląstelių išsiskiria per monokarboksilato transporterius (žinduoliuose MCT 1 ir 2, dar žinomi kaip 16A ištirpusios medžiagos nešėjai 1 ir 7) ir cirkuliacijoje gabenami į ekstrahepatinius audinius galutiniam oksidavimui (Cotter ir kt., 2011; Halestrap ir Wilson, 2012; Halestrap, 2012; Hugo ir kt., 2012). Cirkuliuojančių ketoninių kūnų koncentracijos yra didesnės nei ekstepepatiniuose audiniuose (Harrison ir Long, 1940), o tai rodo, kad ketonų kūnai pernešami koncentracijos gradientu. MCT1 funkcijos praradimo mutacijos yra susijusios su spontaniškomis ketoacidozės priepuoliais, o tai rodo kritinį vaidmenį importuojant ketonus.
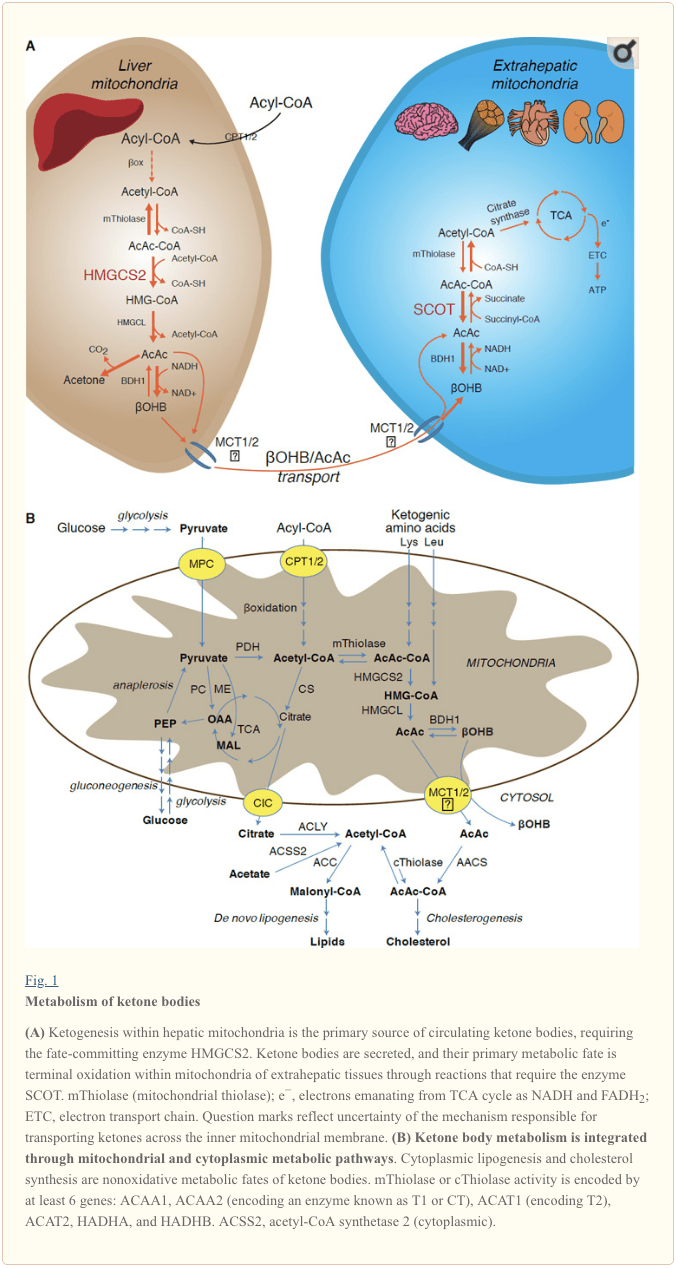
Išskyrus galimą ketoninių kūnų nukreipimą į neoksidacinius likimus (žr. Neoksidaciniai metaboliniai ketoninių kūnų likimai), hepatocitams trūksta galimybės metabolizuoti jų gaminamus ketoninius kūnus. Kepenų de novo sintezuojami ketoniniai kūnai (i) ekstepepatinių audinių mitochondrijose katabolizuojami iki acetil-CoA, kuris yra TCA ciklo galinei oksidacijai (1A pav.), (Ii) nukreipiamas į lipogenezės ar sterolių sintezės kelius ( 1B pav.) Arba (iii) išsiskiria su šlapimu. Kaip alternatyvus energinis kuras ketoniniai kūnai greitai oksiduojasi širdyje, griaučių raumenyse ir smegenyse (Balasse ir Fery, 1989; Bentourkia ir kt., 2009; Owen ir kt., 1967; Reichard ir kt., 1974; Sultan, 1988). ). Ekstrahepatinis mitochondrijų BDH1 katalizuoja pirmąją? OHB oksidacijos reakciją, paversdamas ją atgaline AcAc (LEHNINGER ir kt., 1960; Sandermann ir kt., 1986). Citoplazminė d-? OHB-dehidrogenazė (BDH2), kurios seka identiška tik 20% BDH1, turi didelį ketoninių kūnų Km, taip pat vaidina svarbų vaidmenį geležies homeostazėje (Davuluri ir kt., 2016; Guo ir kt., 2006). . Ekstrepepatinėje mitochondrijų matricoje AcAc aktyvuojamas į AcAc-CoA keičiantis CoA fragmentu iš sukcinil-CoA reakcijoje, kurią katalizuoja unikali žinduolio CoA transferazė, sukcinil-CoA: 3-okso rūgštis-CoA transferazė (SCOT, CoA transferazė; koduojamas OXCT1), vykstant beveik pusiausvyros reakcijai. Laisva energija, išsiskirianti hidrolizuojant AcAc-CoA, yra didesnė už sukcinil-CoA energiją, o tai skatina AcAc susidarymą. Taigi ketono kūno oksidacinis srautas atsiranda dėl masinio veikimo: gausus AcAc tiekimas ir greitas acetil-CoA vartojimas per citratų sintazę skatina AcAc-CoA (+ sukcinato) susidarymą SCOT. Pažymėtina, kad priešingai nei gliukozė (heksokinazė) ir riebalų rūgštys (acil-CoA sintetazės), ketoninių kūnų (SCOT) aktyvavimui į oksiduojamą formą nereikia investuoti į ATP. Grįžtama AcAc-CoA tiolazės reakcija [katalizuojama bet kurios iš keturių mitochondrijų tiolazių, kurias koduoja ACAA2 (koduojantis fermentą, žinomą kaip T1 arba CT), ACAT1 (koduojantis T2), HADHA arba HADHB], gaunamos dvi acetil-CoA molekulės, kurie patenka į TCA ciklą (Hersh ir Jencks, 1967; Stern ir kt., 1956; Williamsonas ir kt., 1971). Ketotinių būsenų metu (t. Y. Bendras ketonų kiekis serume> 500 µM) ketoniniai kūnai tampa reikšmingu energijos sąnaudų indėliu ir yra greitai naudojami audiniuose, kol pasisavinama arba prisotinama oksidacijos (Balasse ir kt., 1978; Balasse ir Fery, 1989 ; Edmond ir kt., 1987). Šlapime galima lengvai išmatuoti labai mažą kepenų darinių kūną, o inkstų panaudojimas ir reabsorbcija yra proporcingi cirkuliuojančiai koncentracijai (Goldstein, 1987; Robinson ir Williamson, 1980). Esant labai ketotinėms būsenoms (> 1 mM plazmoje), ketonurija yra pusiau kiekybinis ketozės reporteris, nors dauguma šlapimo ketoninių kūnų tyrimų nustato AcAc, bet ne? OHB (Klocker et al., 2013).
Ketogeniniai substratai ir jų įtaka hepatocitų metabolizmui
Ketogeninėse substratose yra riebalų rūgščių ir amino rūgščių (1B pav.). Aminorūgščių, ypač leucino, katabolizmas generuoja apie 4% ketoninių kūnų po absorbcijos būsenos (Thomas et al., 1982). Taigi, acetil-CoA substrato baseinas generuoti ketoninius kūnus daugiausia gaunamas iš riebalų rūgščių, nes per mažesnio angliavandenių kiekio būsenoje piruvatas patenka į TCA kepenų ciklą, pirmiausia per anaplerozę, ty nuo ATP priklausančio karboksilinimo iki oksaloacetato (OAA) arba į malatą (MAL), o ne oksidacinis dekarboksilinimas iki acetil-CoA (Jeoung ir kt., 2012; Magnusson ir kt., 1991; Merritt ir kt., 2011). Kepenose gliukozė ir piruvatas nepakankamai prisideda prie ketogenezės, net kai piruvato dekarboksilinimas iki acetil-CoA yra didžiausias (Jeoung ir kt., 2012).
Acetyl-CoA priskiriama keletą vaidmenų, neatsiejamų nuo kepenų tarpinio metabolizmo už ATP generavimo per terminalo oksidaciją (taip pat žr. Ketoninio kūno metabolizmo integravimas, post-transliacijos modifikavimas ir ląstelių fiziologija). Acetyl-CoA alosteririškai aktyvuoja (i) piruvato karboksilazę (PC), taip aktyvuodamas metabolizmo valdymo mechanizmą, kuris didina anaplerozinį metabolitų patekimą į TCA ciklą (Owen ir kt., 2002, Scrutton ir Utter, 1967) ir (ii) piruvatdehidrogenazės kinazę, kuri fosforilina ir slopina piruvatdehidrogenazę (PDH) (Cooper ir kt., 1975), taip dar labiau sustiprinant piravato srautą į TCA ciklą per anaplerozę. Be to, citoplazminis acetil-CoA, kurio baseinas yra papildytas mechanizmais, kurie virsta mitochondrijų acetil-CoA į gabenamus metabolitus, slopina riebiųjų rūgščių oksidaciją: acetil-CoA karboksilazė (ACC) katalizuoja acetil-CoA konversiją malonil-CoA, lipogeninį substratą ir alosterinis mitochondrijų CPT1 inhibitorius [peržiūrėtas (Kahn ir kt., 2005; McGarry ir Foster, 1980)]. Taigi, mitochondrijų acetil-CoA baseinas tiek reguliuojamas, tiek reguliuojamas ketogenezės plitimo keliu, kuris organizuoja pagrindinius kepenų tarpinio metabolizmo aspektus.
Neoksidaciniai metaboliniai kraujo kūnelių likimai
Vyraujantis kepenų kilmės ketonų likimas yra nuo SCOT priklausomas ekstrahapatinis oksidavimas. Tačiau AcAc gali būti eksportuojamas iš mitochondrijų ir panaudojamas anaboliniais būdais per konvertavimą į AcAc-CoA ATP priklausoma reakcija, kurią katalizuoja citoplazminė acetoacetyl-CoA sintetazė (AACS, 1B pav.). Šis būdas yra aktyvus smegenų vystymosi metu ir pieno laktacijos metu (Morris, 2005, Robinson ir Williamson, 1978, Ohgami ir kt., 2003). AACS taip pat labai išreikštas riebaliniu audiniu ir aktyvuotais osteoklatais (Aguilo ir kt., 2010; Yamasaki ir kt., 2016). Citoplazminis AcAc-CoA gali būti nukreiptas į citozolinį HMGCS1 link sterolio biosintezės arba suskaidytas bet kuriuo iš dviejų citoplazminių tiolatų į acetil-CoA (ACAA1 ir ACAT2), karboksilintas su malonil-CoA, ir prisideda prie riebalų rūgščių sintezės (Bergstrom et al., 1984, Edmond, 1974, Endemann ir kt., 1982, Geelen ir kt., 1983, Webber ir Edmond, 1977).
Nors fiziologinė reikšmė dar nenustatyta, ketonai gali būti anaboliniai substratai net kepenyse. Dirbtiniuose eksperimentiniuose kontekstuose AcAc gali sudaryti net pusę naujai susintetintų lipidų ir iki 75% naujo sintetinto cholesterolio (Endemann ir kt., 1982; Geelenas ir kt., 1983; Freedas ir kt., 1988). Kadangi AcAc gaunamas iš neužbaigtos kepenų riebalų oksidacijos, AcAc gebėjimas prisidėti prie lipogenezės in vivo reikštų nenaudingą kepenų ciklą, kai lipidų gamybai gali būti naudojami riebaliniai ketonai, o fiziologinė reikšmė reikalauja eksperimentinio patvirtinimo, tačiau gali būti naudinga prisitaikantys ar netinkamai prisitaikantys vaidmenys (Solinas ir kt., 2015). AcAc greitai teikia cholesterogenezę, turėdamas mažą AACS Km-AcAc (~ 50 µM), skatinantį AcAc aktyvaciją net maitinant (Bergstrom et al., 1984). Dinaminis citoplazminio ketonų metabolizmo vaidmuo buvo pasiūlytas pirminiuose pelių embrioniniuose neuronuose ir 3T3-L1 išvestiniuose-adipocituose, nes AACS nokdaunas sutrikdė kiekvieno ląstelių tipo diferenciaciją (Hasegawa et al., 2012a; Hasegawa et al., 2012b). AACS nukritimas pelėms in vivo sumažino cholesterolio kiekį serume (Hasegawa ir kt., 2012c). SREBP-2, pagrindinis cholesterolio biosintezės transkripcijos reguliatorius ir peroksisomos proliferatoriaus aktyvuotas receptorius (PPAR) -? yra AACS transkripcijos aktyvatoriai ir reguliuoja jos transkripciją vystantis neuritams ir kepenyse (Aguilo ir kt., 2010; Hasegawa ir kt., 2012c). Apibendrinant, citoplazminio ketono organizmo metabolizmas gali būti svarbus esant tam tikroms sąlygoms ar esant natūraliai ligos istorijai, tačiau jų nepakanka išmesti iš kepenų gautus ketoninius kūnus, nes selektyviai sutrikus pirminiam oksidaciniam likimui dėl funkcinių mutacijų praradimo atsiranda didžiulė hiperketonemija. į SCOT (Berry ir kt., 2001; Cotter ir kt., 2011).
HMGCS2 ir SCOT / OXCT1 reguliavimas
Mitochondrijų nukrypimas nuo geno, koduojančio citozolinį HMGCS, atsirado ankstyvoje stuburo vystymosi stadijose dėl poreikio palaikyti kepenų ketogenezę rūšyse, turinčiose didesnį smegenų ir kūno svorio santykį (Boukaftane et al., 1994; Cunnane ir Crawford, 2003). Natūraliai pasitaikanti HMGCS2 mutacija žmonėms sukelia hipoketinės hipoglikemijos pasireiškimą (Pitt ir kt., 2015; Thompson ir kt., 1997). Tvirta HMGCS2 ekspresija yra tik hepatocitų ir storosios žarnos epitelio, o jos raiška ir fermentinis aktyvumas yra koordinuojami įvairiais mechanizmais (Mascaro ir kt., 1995, McGarry ir Foster, 1980, Robinson ir Williamson, 1980). Nors visiškas fiziologinių būsenų, turinčių įtakos HMGCS2, apimtis reikalauja tolesnio išsiaiškinimo, jo raiška ir (arba) aktyvumas yra reguliuojami ankstyvojo postnatalinio periodo metu, senėjimo, diabeto, bado ar ketogeninės dietos nurijus (Balasse ir Fery, 1989, Cahill GF Jr, 2006 , Girard ir kt., 1992; Hegardt, 1999; Satapati ir kt., 2012; Sengupta ir kt., 2010). Hmgcs5 geno 2-ojo šoninio regiono metilinimas vaisiui atvirkščiai koreliuoja su jo transkripcija ir yra iš dalies pakeistas po gimimo (Arias et al., 1995; Ayte et al., 1993; Ehara et al., 2015; Ferre et al. ., 1983). Panašiai, kepenų Bdh1 pasireiškė vystymosi ekspresijos modelis, padidėjęs nuo gimimo iki atjunkymo, taip pat jis buvo sukeltas ketogenine dieta fibroblasto augimo faktoriaus (FGF) -21 priklausomuoju būdu (Badmanas ir kt., 2007; Zhang ir kt., 1989 ) Žinduolių ketogenezė labai reaguoja tiek į insuliną, tiek į gliukagoną, yra slopinama ir stimuliuojama atitinkamai (McGarry ir Foster, 1977). Insulinas slopina riebalinio audinio lipolizę, todėl atimama jo pagrindo ketogenezė, o gliukagonas padidina ketogeninį srautą, tiesiogiai veikdamas kepenis (Hegardt, 1999). Hmgcs2 transkripciją skatina inkstų transkripcijos faktorius FOXA2, kuris slopinamas per insulino fosfatidilinozitolio-3-kinazę / Akt, ir yra indukuojamas gliukagono-cAMP-p300 signalizacijos būdu (Arias ir kt., 1995; Hegardt, 1999; Quant et al. , 1990; Thumelin ir kt., 1993; von Meyenn ir kt., 2013; Wolfrum ir kt., 2004; Wolfrum ir kt., 2003). PPAR? (Rodriguez et al., 1994) kartu su savo taikiniu FGF21 (Badman ir kt., 2007) taip pat skatina Hmgcs2 transkripciją kepenyse badaujant ar vartojant ketogeninę dietą (Badman et al., 2007; Inagaki et al., 2007 ). PPAR indukcija? gali pasireikšti prieš perėjimą nuo vaisiaus prie naujagimio fiziologijos, tuo tarpu FGF21 aktyvacija gali būti palanki ankstyvuoju naujagimių periodu per OHOH sukeltą histono deacetilazės (HDAC) -3 slopinimą (Rando ir kt., 2016). mTORC1 (rapamicino komplekso 1 žinduolių taikinys) priklausomas PPAR slopinimas? transkripcijos aktyvumas taip pat yra pagrindinis Hmgcs2 geno ekspresijos reguliatorius (Sengupta et al., 2010), o kepenų PER2, pagrindinis paros osciliatorius, netiesiogiai reguliuoja Hmgcs2 ekspresiją (Chavan et al., 2016). Naujausi stebėjimai rodo, kad ekstrahepatinio naviko sukeltas interleukinas-6 pažeidžia ketogenezę per PPAR? slopinimas (Flintas ir kt., 2016).
HMGCS2 fermento aktyvumas reguliuojamas per daugelį PTM. HMGCS2 serino fosforilinimas padidino savo aktyvumą in vitro (Grimsrud ir kt., 2012). HMGCS2 aktyvumą allosteriškai slopina succinil-CoA ir lizino liekanų sukcinilinimas (Arias ir kt., 1995; Hegardt, 1999; Lowe ir Tubbs; 1985; Quant ir kt., 1990; Rardin ir kt., 2013; Reed et al. 1975; Thumelin ir kt., 1993). HMGCS2, HMGCL ir BDH1 lizino likučių nuosėdų susikaupimas kepenų mitochondrijose yra NAD + priklausomos deacilazės sirtuino 5 (SIRT5) (Rardin ir kt., 2013) tikslai. HMGCS2 aktyvumą taip pat stiprina lizino dezetilinimas SIRT3, ir yra įmanoma, kad tarp acetilinimo ir sukcinilinimo atsirandantis silpnumas reguliuoja HMGCS2 aktyvumą (Rardin ir kt., 2013; Shimazu ir kt., 2013). Nepaisant šių PTM sugebėjimų reguliuoti HMGCS2 Km ir Vmax, šių PTM svyravimai dar nebuvo tiksliai susisteminti ir nebuvo patvirtinti kaip mechaniniai ketogenezės varikliai in vivo.
SCOT išreiškiamas visose žinduolių ląstelėse, kuriose yra mitochondrijų, išskyrus hepatocitus. SCOT aktyvumo ir ketolizės svarba buvo įrodyta SCOT-KO pelėse, kurios pasireiškė vienodu mirtingumu dėl hiperketoneminės hipoglikemijos per 48h po gimimo (Cotter ir kt., 2011). SCOT netekimas audiniuose neuronuose ar skeleto miocituose sukelia medžiagų apykaitos sutrikimus bado metu, bet nėra mirtina (Cotter et al., 2013b). Žmonėms SCOT trūkumas ankstyvoje gyvenimo stadijoje rodo sunkią ketoacidozę, sukeliančią letargiją, vėmimą ir komą (Berry ir kt., 2001; Fukao ir kt., 2000; Kassovska-Bratinova ir kt., 1996; Niezen-Koning et ai. , 1997, Saudubray ir kt., 1987, Snyderman ir kt., 1998, Tildon ir Cornblath, 1972). Santykinai mažai žinoma ląstelių lygyje apie SCOT geną ir baltymų ekspresijos reguliatorius. Oxct1 mRNR ekspresija ir SCOT baltymas ir aktyvumas mažėja ketotinėse būsenose, galbūt per PPAR priklausomus mechanizmus (Fenselau ir Wallis, 1974, Fenselau ir Wallis, 1976, Grinblat ir kt., 1986, Okuda ir kt., 1991, Turko et al ., 2001; Wentz ir kt., 2010). Diabetinė ketoacidozė susilpnina SCOT aktyvumo sutrikimą, nes skiriasi kepenų ketogenezė ir ekstrahepatinė oksidacija. Iš insulino nepriklausančio gliukozės transporterio (GLUT1 / SLC2A1) per didelio ekspresavimo kardiomiukai taip pat slopina Oxct1 geno ekspresiją ir mažina ketonų terminį oksidavimą ne ketoticinėje būsenoje (Yan et al., 2009). Keptuose Oxct1 mRNR kiekį slopina microRNA-122 ir histono metilinimas H3K27me3, kurie yra akivaizdūs pereinant nuo vaisiaus iki naujagimio laikotarpio (Thorrez ir kt., 2011). Tačiau kepenų Oxct1 ekspresijos slopinimas po gimimo yra visų pirma susijęs su Oxct1 ekspresuojančių hematopoetinių progenorių evakacija iš kepenų, o ne anksčiau egzistuojančios Oxct1 išraiškos praradimas nenuosekliai diferencijuotose hepatocitose. Iš tiesų, Oxct1 mRNR ir SCOT baltymo ekspresija diferencijuotose hepatocitose yra labai maža (Orii ir kt., 2008).
SCOT taip pat reguliuoja PTM. Fermentas yra hiperacetilintas SIRT3 KO pelių smegenyse, kurios taip pat rodo sumažėjusią AcAc priklausomą acetil-CoA gamybą (Dittenhafer-Reed ir kt., 2015). Ne fermentinis SCOT tirozino likučių nitrinimas taip pat silpnina jo aktyvumą, apie kurį pranešta įvairių diabetinių pelių modelių širdyse (Marcondes et al., 2001; Turko et al., 2001; Wang et al., 2010a). Priešingai, triptofano likučių nitrinimas padidina SCOT aktyvumą (Br g re et al., 2010; Rebrin et al., 2007). Gali egzistuoti molekuliniai liekanų specifinio nitratymo arba nitratinimo mechanizmai, skirti moduliuoti SCOT aktyvumą, ir juos reikia išaiškinti.
Neutraliosios ketogenezės ginčai
Žinduoliuose pagrindinis ketogeninis organas yra kepenys, o tik hepatocitai ir žarnos epitelio ląstelės gausiai ekspresuoja HMGCS2 mitochondrijų izoformą (Cotter et al., 2013a; Cotter et al., 2014; McGarry and Foster, 1980; Robinson and Williamson, 1980). . Anaerobinė bakterinė kompleksinių polisacharidų fermentacija duoda butiratą, kurį kolonocitai absorbuoja žinduoliuose, kad gautų galinę oksidaciją ar ketogenezę (Cherbuy ir kt., 1995), kurie gali vaidinti vaidmenį kolonocitų diferenciacijoje (Wang ir kt., 2016). Išskyrus žarnyno epitelio ląsteles ir hepatocitus, HMGCS2 beveik nėra beveik visose kitose žinduolių ląstelėse, tačiau ekstepepatinės ketogenezės galimybė buvo iškelta naviko ląstelėse, centrinės nervų sistemos astrocituose, inkstuose, kasoje? ląstelių, tinklainės pigmento epitelio (RPE) ir net griaučių raumenyse (Adijanto et al., 2014; Avogaro et al., 1992; El Azzouny et al., 2016; Grabacka et al., 2016; Kang et al., 2015 ; Le Foll ir kt., 2014; Nonaka ir kt., 2016; Takagi ir kt., 2016a; Thevenet ir kt., 2016; Zhang ir kt., 2011). Negimdinis HMGCS2 buvo pastebėtas audiniuose, kuriuose nėra grynojo ketogeninio pajėgumo (Cook ir kt., 2016; Wentz ir kt., 2010), o HMGCS2 rodo perspektyvią nuo ketogenezės nepriklausančią „mėnulio apšvietimo“ veiklą, įskaitant ląstelės branduolį (Chen ir kt. , 2016; Kostiuk ir kt., 2010; Meertens ir kt., 1998).
Bet koks ketepinius kūnus oksiduojantis ekstrahepatinis audinys taip pat gali kaupti ketoninius kūnus per HMGCS2 nepriklausomus mechanizmus (2A pav.). Tačiau nėra jokio ekstepepatinio audinio, kuriame pastovaus ketono kūno koncentracija viršytų kraujotakoje esančią koncentraciją (Cotter et al., 2011; Cotter et al., 2013b; Harrison and Long, 1940), pabrėžiant, kad ketono kūnai yra transportuojami žemyn. koncentracijos gradientas per MCT1 / 2 priklausomus mechanizmus. Vienas akivaizdžios ekstrahepatinės ketogenezės mechanizmas iš tikrųjų gali atspindėti santykinį ketonų oksidacijos pažeidimą. Papildomi galimi paaiškinimai patenka į ketonų kūno formavimo sritį. Pirma, de novo ketogenezė gali atsirasti dėl grįžtamojo tiolazės ir SCOT fermentinio aktyvumo (Weidemann ir Krebs, 1969). Kai acetil-CoA koncentracija yra santykinai didelė, reakcijos, paprastai atsakingos už AcAc oksidaciją, veikia atvirkštine kryptimi (GOLDMAN, 1954). Antrasis mechanizmas įvyksta, kai dėl TCA ciklo kliūties kaupiasi a-oksidacijos būdu gauti tarpiniai produktai, AcAc-CoA paverčiamas l-? OHB-CoA per reakciją, kurią katalizuoja mitochondrijų 3-hidroksiacil-CoA dehidrogenazė, o toliau - 3-hidroksibutirilas. CoA deacilazė iki 1980-OHB, kuri masių spektrometrija ar rezonanso spektroskopija niekuo neišsiskiria iš fiziologinio enantiomero d-OHH (Reed ir Ozand, 2011). l-? OHB galima chromatografiškai arba fermentiškai atskirti nuo d-? OHB ir yra ekstepepatiniuose audiniuose, bet ne kepenyse ar kraujyje (Hsu ir kt., 1984). Kepenų ketogenezė gamina tik d-? OHB, vienintelį enantiomerą, kuris yra BDH substratas (Ito ir kt., 1987; Lincoln ir kt., 1980; Reed ir Ozand, 1982; Scofield ir kt., 1982; Scofield ir kt., 2). Trečiasis nuo HMGCS1990 nepriklausomas mechanizmas generuoja d-OHB dėl aminorūgščių, ypač leucino ir lizino, katabolizmo. Ketvirtasis mechanizmas yra akivaizdus tik todėl, kad jis yra dėl žymėjimo artefakto ir todėl vadinamas pseudoketogeneze. Šis reiškinys siejamas su SCOT ir tiolazės reakcijų grįžtamumu ir gali pervertinti ketonų kūno apykaitą dėl izotopinio ketoninio kūno žymeklio praskiedimo ekstrahepatiniame audinyje (Des Rosiers et al., 1988; Fink et al., 1990) . Nepaisant to, pseudoketogenezė daugumoje kontekstų gali būti nereikšminga (Bailey ir kt., 1978; Keller ir kt., 2). Schema (XNUMXA pav.) Rodo naudingą metodą, kurį reikia taikyti, atsižvelgiant į padidėjusią ketonų koncentraciją audiniuose.
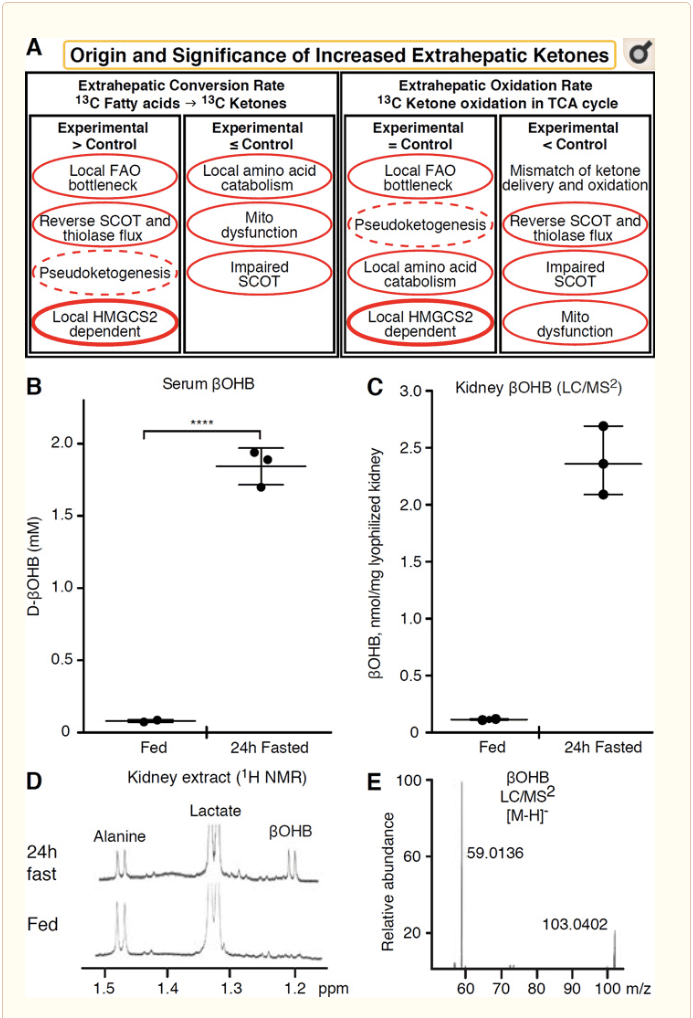

Inkstai pastaruoju metu sulaukė dėmesio kaip potencialiai ketogeninis organas. Daugumoje valstybių inkstai yra pagrindinis kepenų ketoninių kūnų vartotojas, išskiriantis ar absorbuojantis ketoninius kūnus iš kraujotakos, o inkstai paprastai nėra grynasis ketoninio kūno generatorius ar koncentratorius (Robinson ir Williamson, 1980). Klasikinio tyrimo autoriai padarė išvadą, kad minimali inkstų ketogenezė, apskaičiuota dirbtinėje eksperimentinėje sistemoje, nėra fiziologiškai reikšminga (Weidemann ir Krebs, 1969). Neseniai inkstų ketogenezė buvo nustatyta remiantis diabetinių ir autofagijos deficito pelių modeliais, tačiau labiau tikėtina, kad daugelio organų poslinkiai metabolinėje homeostazėje keičia integracinę ketonų apykaitą per daugelio organų įnašus (Takagi et al., 2016a; Takagi et al., 2016b; Zhang ir kt., 2011). Vienoje neseniai paskelbtoje publikacijoje inkstų ketogenezė buvo siūloma kaip apsauginis mechanizmas nuo išemijos-reperfuzijos pažeidimo inkstuose (Tran ir kt., 2016). Buvo pranešta apie absoliučią pastovios koncentracijos β OHB koncentraciją iš pelių inkstų audinio ekstraktų esant ~ 4 mM. Norėdami patikrinti, ar tai buvo tinkama, kiekybiškai įvertinome? OHB koncentraciją inkstų ekstraktuose iš maitintų ir 12 valandas nevalgiusių pelių. Serumo OHH koncentracija padidėjo nuo ~ 24 µM iki 100 mM nevalgius 2 valandas (24B pav.), O pastovi inkstų būsena OH OHB koncentracija buvo apytiksliai 2 µM maitinamoje būsenoje ir tik 100 mM 1 valandų nevalgius (pav. 24C E), stebėjimai, atitinkantys koncentracijas, apskaičiuotas daugiau nei prieš 2 metus (Hems ir Brosnan, 45). Lieka įmanoma, kad esant ketozinėms būsenoms, iš kepenų gaunami ketoniniai kūnai gali būti renoprotekciniai, tačiau inkstų ketogenezės įrodymai reikalauja tolesnio pagrindimo. Įtikinami įrodymai, patvirtinantys tikrąją ekstepepatinę ketogenezę, buvo pateikti RPE (Adijanto ir kt., 1970). Buvo pasiūlyta ši intriguojanti metabolinė transformacija, leidžianti leisti RPE gautiems ketonams tekėti į fotoreceptoriaus arba M.ller glia ląsteles, o tai galėtų padėti regeneruoti fotoreceptoriaus išorinį segmentą.
OHB kaip signalizavimo tarpininkas
Nors jie yra energetiškai turtingi, ląstelių homeostazėje ketoniniai kūnai atlieka provokuojančius „ne kanoninius“ signalizavimo vaidmenis (3 pav.) (Newman ir Verdin, 2014; Rojas-Morales ir kt., 2016). Pvz.,? OHB slopina I klasės HDAC, o tai padidina histono acetilinimą ir taip sukelia genų, kurie mažina oksidacinį stresą, ekspresiją (Shimazu ir kt., 2013). Pats OHB yra histono kovalentinis modifikatorius lizino likučiuose nevalgiusių ar streptozotocino sukeltų diabetinių pelių kepenyse (Xie ir kt., 2016) (taip pat žr. Žemiau, Ketonų kūno metabolizmo integravimas, modifikavimas po transliacijos ir ląstelių fiziologija) Ketoniniai kūnai, oksidacinis stresas ir neuroprotekcija).
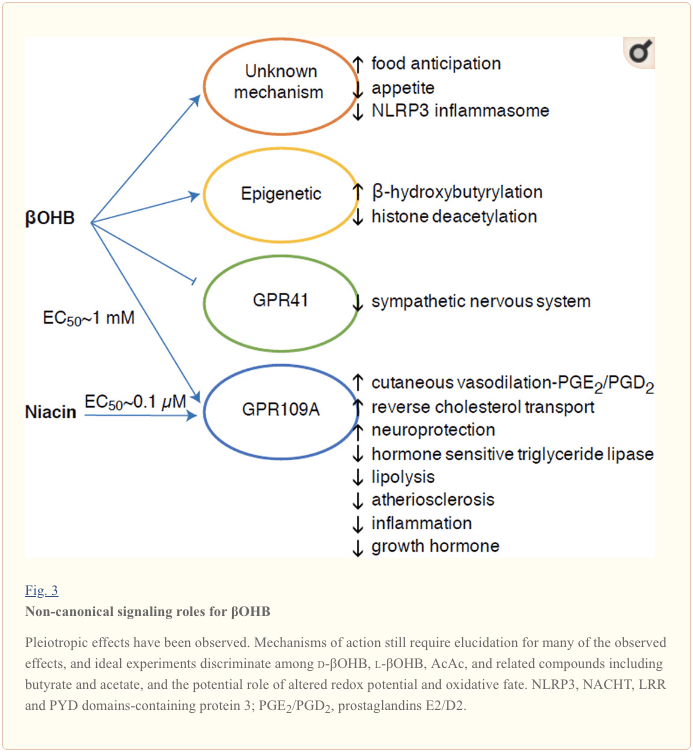
OHB taip pat yra efektorius per G-baltymus sujungtus receptorius. Naudodamas neaiškius molekulinius mechanizmus, jis slopina simpatinės nervų sistemos aktyvumą ir sumažina bendrą energijos sąnaudas bei širdies susitraukimų dažnį, slopindamas trumpųjų grandinių riebalų rūgščių signalizaciją per G baltymu susietą receptorių 41 (GPR41) (Kimura ir kt., 2011). Vienas iš labiausiai ištirtų? OHB signalinių efektų vyksta per GPR109A (taip pat žinomą kaip HCAR2), hidrokarboksirūgšties GPCR pogrupio narį, išreikštą riebaliniuose audiniuose (baltos ir rudos spalvos) (Tunaru ir kt., 2003) ir imuninės ląstelės (Ahmed et al., 2009). -OHB yra vienintelis žinomas endogeninis GPR109A receptoriaus (EC50 ~ 770 µM) ligandas, kurį aktyvuoja d- OHOH, 2005-OHBB ir butiratas, bet ne AcAc (Taggart ir kt., 109). Aukšta GPR109A aktyvacijos koncentracijos riba pasiekiama laikantis ketogeninės dietos, badaujant ar ketoacidozės metu, dėl ko slopinamas riebalinio audinio lipolizė. Antilipolitinis GPR2009A poveikis vyksta slopinant adenililo ciklazę ir sumažinus cAMP, slopinant jautrias hormonams trigliceridų lipazes (Ahmed et al., 2003; Tunaru et al., 2009). Tai sukuria neigiamą grįžtamojo ryšio ciklą, kuriame ketozė stabdo moduliacinį ketogenezės stabdymą, mažindama esterifikuotų riebalų rūgščių išsiskyrimą iš adipocitų (Ahmed et al., 2005; Taggart et al., 3), kurį gali atsverti simpatinis potraukis, stimuliuojantis lipolizę. Niacinas (vitaminas B50, nikotino rūgštis) yra stiprus (EC0.1 ~ 109 µM) ligandas GRP2005A, dešimtmečius veiksmingai vartojamas dislipidemijų atveju (Benyo ir kt., 2006; Benyo ir kt., 2010; Fabbrini ir kt., 2011a; Lukasova ir kt., 2003; Tunaru ir kt., 2011). Nors niacinas sustiprina atvirkštinį cholesterolio pernašą makrofaguose ir sumažina aterosklerozinius pažeidimus (Lukasova ir kt., 109), „OHB“ poveikis ateroskleroziniams pažeidimams lieka nežinomas. Nors GPR2015A receptorius atlieka apsauginius vaidmenis ir yra intriguojančių ryšių tarp ketogeninės dietos vartojimo sergant insultu ir neurodegeneracinių ligų (Fu ir kt., 2014; Rahman ir kt., 109), apsauginis? OHB vaidmuo per GPRXNUMXA nebuvo įrodytas in vivo .
Pagaliau? OHB gali paveikti apetitą ir sotumą. Tyrimų, kuriuose buvo matuojamas ketogeninių ir labai mažai energijos turinčių dietų poveikis, metaanalizė padarė išvadą, kad dalyviai, vartojantys šias dietas, pasižymi didesniu sotumu, palyginti su kontrolinėmis dietomis (Gibson ir kt., 2015). Tačiau tikėtinas šio poveikio paaiškinimas yra papildomi metaboliniai ar hormoniniai elementai, kurie gali moduliuoti apetitą. Pavyzdžiui, pelėms, laikomoms graužikų ketogeninės dietos, nepaisant panašaus kalorijų kiekio, energijos sąnaudos buvo didesnės, palyginti su pelėmis, kurios buvo maitinamos kontroliniu būdu, nepaisant panašaus kalorijų kiekio, o cirkuliuojantis leptinas ar maitinimo elgesį reguliuojantys peptidų genai nebuvo pakeisti (Kennedy ir kt., 2007). Tarp siūlomų mechanizmų, kurie rodo apetito slopinimą? OHB, apima signalizaciją ir oksidaciją (Laeger ir kt., 2010). Hepatocitų specifinis cirkadinio ritmo geno (Per2) ir chromatino imunoprecipitacijos ištrynimas parodė, kad PER2 tiesiogiai aktyvina Cpt1a geną ir netiesiogiai reguliuoja Hmgcs2, o tai lemia ketozės pažeidimą Per2 nokautinėse pelėse (Chavan ir kt., 2016). Šioms pelėms buvo sutrikęs maisto laukimas, kurį iš dalies atstatė sisteminis A OHB vartojimas. Būsimi tyrimai bus reikalingi norint patvirtinti, kad centrinė nervų sistema yra tiesioginis? OHB taikinys ir ar ketonams reikia oksiduotis dėl pastebėto poveikio, ar yra naudojamas kitas signalizavimo mechanizmas. Kiti tyrėjai nurodė vietinės astrocitų kilmės ketogenezės galimybę ventromedialiniame hipotalamyje kaip maisto reguliatorių, tačiau šiems išankstiniams stebėjimams taip pat bus naudinga genetiniais ir srautu pagrįstais vertinimais (Le Foll ir kt., 2014). Ryšys tarp ketozės ir maistinių medžiagų trūkumo išlieka įdomus, nes alkis ir sotumas yra svarbūs nepavykusių svorio metimo elementai.
Ketoninės kūno metabolizmo integravimas, transliacinis modifikavimas ir ląstelių fiziologija
Ketoniniai organai prisideda prie acetil-CoA, pagrindinio tarpinio junginio, kuris yra svarbus ląstelių metabolizmo vaidmuo, suskaidyti (Pietrocola et al., 2015). Acetil-CoA vaidmuo yra acetilinimo, fermentuoto katalizuojamo histologinio kovalentinio modifikavimo substratas (Choudhary ir kt., 2014; Dutta ir kt., 2016; Fan ir kt., 2015; Menzies ir kt., 2016 ) Daugybė dinamiškai acetilintų mitochondrijų baltymų, daugelis iš jų gali atsirasti per nefermentinius mechanizmus, taip pat atsirado iš skaičiavimo proteomikos tyrimų (Dittenhafer-Reed ir kt., 2015, Hebert ir kt., 2013, Rardin ir kt., 2013 ; Shimazu ir kt., 2010). Lizino deacetilazės naudoja cinko kofaktorių (pvz., Nukleocitozolinius HDAC) arba NAD + kaip bendrą substratą (sirtuinai, SIRT) (Choudhary ir kt., 2014; Menzies ir kt., 2016). Acetilproteomas yra tiek viso junginio acetil-CoA baseino daviklis, tiek efektorius, nes kiekvieno fiziologinio ir genetinio manipuliavimo rezultatai yra nefermentiniai globalūs acetilinimo variantai (Weinert ir kt., 2014). Kadangi intracellular metabolites tarnauja kaip lizino likučių acetilinimo moduliatoriai, svarbu atsižvelgti į ketoninių kūnų, kurių gausumas yra labai dinamiškas, vaidmenį.
OHB yra epigenetinis modifikatorius, veikiantis mažiausiai dviem mechanizmais. Padidėjęs? OHB lygis, kurį sukelia nevalgymas, kalorijų apribojimas, tiesioginis vartojimas ar ilgalaikis fizinis krūvis, išprovokuoja HDAC slopinimą ar histono acetiltransferazės aktyvaciją (Marosi ir kt., 2016; Sleimanas ir kt., 2016) arba oksidacinį stresą (Shimazu ir kt., 2013). . • OHAC HDAC3 slopinimas galėtų reguliuoti naujagimio metabolinę fiziologiją (Rando ir kt., 2016). Nepriklausomai, pats OHB tiesiogiai modifikuoja histono lizino liekanas (Xie ir kt., 2016). Ilgai nevalgius arba steptozotocino sukelta diabetinė ketoacidozė padidino histono a-hidroksibutirilinimą. Nors lizino a-hidroksibutirilinimo ir acetilinimo vietų skaičius buvo panašus, pastebėta stechiometriškai didesnė histono a-hidroksibutirilinimo, nei acetilinimo, dalis. Skirtingus genus paveikė histono lizino a-hidroksibutirilinimas, palyginti su acetilinimu ar metilinimu, o tai rodo aiškias ląstelių funkcijas. Ar a-hidroksibutirilinimas yra savaiminis, ar fermentinis, nežinoma, tačiau plečiant mechanizmus, ketoniniai kūnai dinamiškai veikia transkripciją.
Esminiai ląstelių perprogramavimo įvykiai kalorijų apribojimo ir maistinių medžiagų trūkumo metu gali būti tarpininkaujami atitinkamai nuo SIRT3 ir SIRT5 priklausomai nuo mitochondrijų deacetilinimo ir desukcinilinimo, reguliuojant ketogeninius ir ketolitinius baltymus po transliacijos lygmens kepenyse ir papildomuose kepenyse (Dittenhafer-Reed et al. 2015; Hebert ir kt., 2013; Rardin ir kt., 2013; Shimazu ir kt., 2010). Nors užimtų vietų stechiometrinis palyginimas nebūtinai yra tiesiogiai susijęs su metabolinio srauto pokyčiais, mitochondrijų acetilinimas yra dinamiškas ir gali būti nulemtas acetil-CoA koncentracijos ar mitochondrijų pH, o ne fermentinių acetiltransferazių (Wagner ir Payne, 2013). Tai, kad SIRT3 ir SIRT5 moduliuoja ketonus organizmą metabolizuojančių fermentų aktyvumą, sukelia klausimą apie abipusį ketonų vaidmenį formuojant acetilproteomą, sukcinilproteomą ir kitus dinaminius ląstelių taikinius. Iš tiesų, kadangi ketogenezės pokyčiai atspindi NAD + koncentraciją, ketonų gamyba ir gausa gali reguliuoti sirtuino aktyvumą, taip paveikdami bendrą acetil-CoA / sukcinil-CoA telkinius, acilproteomą, taigi ir mitochondrijų bei ląstelių fiziologiją. Fermento lizino liekanų a-hidroksibutirilinimas gali papildyti ląstelių perprogramavimą dar vienu sluoksniu. Ekstepatiniuose audiniuose ketonų kūno oksidacija gali stimuliuoti analogiškus ląstelių homeostazės pokyčius. Nors acetil-CoA telkinių skirstymas yra labai reguliuojamas ir koordinuoja platų ląstelių pokyčių spektrą, ketoninių kūnų gebėjimas tiesiogiai formuoti tiek mitochondrijų, tiek citoplazminių acetil-CoA koncentracijas reikalauja išsiaiškinti (Chen ir kt., 2012; Corbet ir kt., 2016; Pougovkina ir kt., 2014; Schwer ir kt., 2009; Wellenas ir Thompsonas, 2012). Kadangi acetil-CoA koncentracija yra griežtai reguliuojama, o acetil-CoA yra nepralaidus membranai, labai svarbu atsižvelgti į varomuosius mechanizmus, koordinuojančius acetil-CoA homeostazę, įskaitant gamybos greitį ir galutinę oksidaciją TCA cikle, virsmą į ketoninius kūnus, mitochondriją. ištekėjimas per karnitino acetiltransferazę (CrAT) arba acetil-CoA eksportas į citozolį po pavertimo citratu ir išleidimo ATP citrato liazės (ACLY) pagalba. Pagrindiniai šių pastarųjų mechanizmų vaidmenys ląstelių acetilproteomoje ir homeostazėje reikalauja suderinto ketogenezės ir ketonų oksidacijos vaidmens supratimo (Das ir kt., 2015; McDonnell ir kt., 2016; Moussaieffas ir kt., 2015; Overmyer ir kt., 2015; Seiler ir kt., 2014; Seiler ir kt., 2015; Wellen ir kt., 2009; Wellenas ir Thompsonas, 2012). Norint nurodyti tikslus ir rezultatus, reikės konvergencinių metabolomikos ir acilproteomikos technologijų nustatant genetiškai manipuliuotus modelius.
Antioksidantai ir uždegiminiai atsakymai į ketonines medžiagas
Ketozė ir ketoniniai kūnai moduliuoja uždegimą ir imuninių ląstelių funkciją, tačiau buvo pasiūlyti įvairūs ir netgi neatitikimo mechanizmai. Ilgalaikis maistinių medžiagų trūkumas sumažina uždegimą (Youm ir kt., 2015), tačiau lėtinė 1 tipo diabeto ketozė yra uždegimą skatinanti būsena (Jain ir kt., 2002; Kanikarla-Marie ir Jain, 2015; Kurepa ir kt., 2012 ). Mechanizmu pagrįsti signalo vaidmenys? OHB uždegime atsiranda todėl, kad daugelis imuninės sistemos ląstelių, įskaitant makrofagus ar monocitus, gausiai ekspresuoja GPR109A. Nors? OHB dažniausiai sukelia priešuždegiminį atsaką (Fu ir kt., 2014; Gambhir ir kt., 2012; Rahmanas ir kt., 2014; Youm ir kt., 2015), didelė ketoninių kūnų, ypač AcAc, koncentracija gali sukelti uždegimą skatinantį atsaką (Jain ir kt., 2002; Kanikarla-Marie ir Jain, 2015; Kurepa ir kt., 2012).
Apžvelgti GPR109A ligandų priešuždegiminiai vaidmenys aterosklerozės, nutukimo, uždegiminės žarnų ligos, neurologinių ligų ir vėžio atvejais (Graff ir kt., 2016). GPR109A ekspresija padidėja diabetinių modelių, žmonių, sergančių diabetu, RPE ląstelėse (Gambhir ir kt., 2012) ir mikroglijose neurodegeneracijos metu (Fu ir kt., 2014). Priešuždegiminį? OHB poveikį sustiprina GPR109A perekspresija RPE ląstelėse ir panaikina farmakologinis GPR109A slopinimas arba genetinis nokautas (Gambhir et al., 2012). • OHB ir egzogeninė nikotino rūgštis (Taggart ir kt., 2005) abu sukelia priešuždegiminį poveikį TNF? arba LPS sukeltas uždegimas, sumažinant uždegimą skatinančių baltymų (iNOS, COX-2) arba išskiriamų citokinų (TNFa, IL-1a, IL-6, CCL2 / MCP-1) kiekį, iš dalies slopinant NF -? B translokacija (Fu ir kt., 2014; Gambhir ir kt., 2012). OHB sumažina ER stresą ir NLRP3 uždegimą, suaktyvindamas antioksidacinį streso atsaką (Bae et al., 2016; Youm et al., 2015). Tačiau esant neurodegeneraciniam uždegimui, GPR109A priklausoma apsauga nuo OHB nėra susijusi su uždegimo mediatoriais, tokiais kaip MAPK kelio signalizacija (pvz., ERK, JNK, p38) (Fu ir kt., 2014), tačiau gali prireikti nuo COX-1 priklausomo PGD2 gamyba (Rahman ir kt., 2014). Įdomu tai, kad išeminio insulto modelyje neuroprotekciniam poveikiui pasiekti reikalingas makrofagas GPR109A (Rahman ir kt., 2014), tačiau? OHB gebėjimas slopinti NLRP3 uždegimą kaulų čiulpų makrofaguose yra GPR109A nepriklausomas (Youm et al. ., 2015). Nors dauguma tyrimų susieja „OHB“ su priešuždegiminiu poveikiu, „OHB“ gali būti uždegimą skatinantis ir padidinti veršelių hepatocitų lipidų peroksidacijos žymenis (Shi ir kt., 2014). Taigi anti-priešuždegiminis OH OHB poveikis gali priklausyti nuo ląstelės tipo, OH OH koncentracijos, ekspozicijos trukmės ir ko-moduliatorių buvimo ar nebuvimo.
Skirtingai nuo? OHB, AcAc gali suaktyvinti uždegimą skatinantį signalizavimą. Padidėjęs AcAc, ypač esant didelei gliukozės koncentracijai, sustiprina endotelio ląstelių pažeidimą per NADPH oksidazės / oksidacinio streso priklausomą mechanizmą (Kanikarla-Marie ir Jain, 2015). Didelės AcAc koncentracijos diabetu sergančių motinų virkštelėje buvo susijusios su didesniu baltymų oksidacijos greičiu ir MCP-1 koncentracija (Kurepa ir kt., 2012). Didelis cukriniu diabetu sergančių pacientų AcAc kiekis buvo susijęs su TNF? ekspresija (Jain ir kt., 2002), ir AcAc, bet ne? OHB, sukėlė TNFa, MCP-1 ekspresiją, ROS kaupimąsi ir sumažino cAMP lygį U937 žmogaus monocitų ląstelėse (Jain ir kt., 2002; Kurepa ir kt. ., 2012).
Ketono organizmo priklausomi signalizacijos reiškiniai dažnai pasireiškia tik esant didelei ketonų kūno koncentracijai (> 5 mM), ir daugelio tyrimų atveju, susiejant ketonus su priešuždegiminiu ar priešuždegiminiu poveikiu, naudojant neaiškius mechanizmus. Be to, dėl prieštaringo? OHB, palyginti su AcAc, poveikio uždegimui ir AcAc /? OHB santykio gebėjimo paveikti mitochondrijų redokso potencialą, geriausiuose ketoninių kūnų vaidmens ląstelių fenotipuose įvertinimo eksperimentuose lyginamas AcAc ir? OHB įvairiais santykiais ir skirtingomis kaupiamosiomis koncentracijomis [pvz., (Saito ir kt., 2016)]. Galiausiai, AcAc galima įsigyti komerciškai tik kaip ličio druską arba kaip etilo esterį, kuriam prieš naudojant reikia bazės hidrolizės. Ličio katijonas nepriklausomai sukelia signalo perdavimo kaskadas (Manji ir kt., 1995), o AcAc anijonas yra labilus. Galiausiai, tyrimai, naudojant raceminį d / l-OHOHB, gali būti supainioti, nes tik d-OHOH stereoizomerą galima oksiduoti iki AcAc, tačiau d-? OHB ir l-OHOH gali kiekvienas signalizuoti per GPR109A, slopinti NLRP3 uždegimą, ir tarnauja kaip lipogeniniai substratai.
Ketonų kūnai, oksidacinis stresas ir neuroproteka
Oksidacinis stresas paprastai apibrėžiamas kaip būsena, kai ROS yra per didelis dėl per didelės gamybos ir (arba) sutrikusios eliminacijos. Antioksidaciniai ir oksidacinį stresą mažinantys ketoninių kūnų vaidmenys buvo plačiai aprašyti tiek in vitro, tiek in vivo, ypač neuroprotekcijos kontekste. Kadangi dauguma neuronų efektyviai negamina didelės energijos fosfatų iš riebalų rūgščių, tačiau oksiduoja ketoninius kūnus, kai trūksta angliavandenių, ypač svarbus ketoninių kūnų neuroprotekcinis poveikis (Cahill GF Jr, 2006; Edmond et al., 1987; Yang ir kt., 1987). Vykdant oksidacinio streso modelius, BDH1 indukcija ir SCOT slopinimas rodo, kad ketonų organizmo metabolizmą galima perprogramuoti, kad būtų palaikomas įvairus ląstelių signalizavimas, redokso potencialas ar medžiagų apykaitos poreikiai (Nagao ir kt., 2016; Tieu ir kt., 2003).
Ketoniniai kūnai sumažina ląstelių pažeidimo, sužalojimo, mirties laipsnius ir mažesnę apoptozę neuronuose ir kardiomiocituose (Haces et al., 2008; Maalouf et al., 2007; Nagao et al., 2016; Tieu et al., 2003). Taikomi mechanizmai yra įvairūs ir ne visada tiesiškai susiję su koncentracija. Maža milimolinė (d arba l) - OHOH pašalina ROS (hidroksilo anijoną), tuo tarpu AcAc pašalina daugelį ROS rūšių, tačiau tik esant koncentracijai, viršijančiai fiziologinį diapazoną (IC50 20 mM) (Haces ir kt., 67) . Ir atvirkščiai, naudinga įtaka elektronų perdavimo grandinės redokso potencialui yra mechanizmas, dažniausiai susijęs su d-OHB. Nors visi trys ketoniniai kūnai (d / l-? OHB ir AcAc) sumažino neuronų ląstelių mirtį ir ROS kaupimąsi, kurį sukėlė cheminis glikolizės slopinimas, tik d-? OHB ir AcAc užkirto kelią neuronų ATP mažėjimui. Priešingai, hipoglikeminiame in vivo modelyje (d arba l) - OHOH, bet ne AcAc, užkirto kelią hipokampo lipidų peroksidacijai (Haces et al., 2008; Maalouf et al., 2008; Marosi et al., 2007; Murphy, 2016 ; Tieu ir kt., 2009). In vivo tyrimai su pelėmis, maitinamomis ketogenine dieta (2003% kcal riebalų ir 87% baltymų), parodė neuroanatominius antioksidacinio pajėgumo pokyčius (Ziegler ir kt., 13), kur giliausi pokyčiai buvo pastebėti hipokampe, padidėjus glutationo peroksidazei ir bendrai. antioksidaciniai pajėgumai.
Ketogeninė dieta, ketoniniai esteriai (taip pat žr. Ketogeninės dietos ir egzogeninių ketoninių kūnų terapinis naudojimas) arba? OHB vartojimas išeminio insulto modeliuose apsaugo neuroproteiną (Rahman ir kt., 2014); Parkinsono liga (Tieu ir kt., 2003); centrinės nervų sistemos toksiškumo deguoniui priepuolis (D'Agostino ir kt., 2013); epilepsijos spazmai (Yum ir kt., 2015); mitochondrijų encefalomijopatija, pieno rūgšties acidozė ir į insultą panašūs (MELAS) epizodų sindromas (Frey ir kt., 2016) ir Alzheimerio liga (Cunnane ir Crawford, 2003; Yin ir kt., 2016). Ir atvirkščiai, naujausia ataskaita parodė neuropatologinius neurodegeneracinio progresavimo ketogenine dieta įrodymus nenormalaus mitochondrijų DNR atstatymo transgeniniame pelės modelyje, nepaisant mitochondrijų biogenezės ir antioksidacinių parašų padidėjimo (Lauritzen et al., 2016). Kiti prieštaringi pranešimai rodo, kad didelės ketono koncentracijos organizme sukelia oksidacinį stresą. Didelės? OHB arba AcAc dozės sukėlė azoto oksido sekreciją, lipidų peroksidaciją, sumažino SOD, glutationo peroksidazės ir katalazės raišką veršelių hepatocituose, o žiurkių hepatocituose MAPK kelio indukcija buvo priskirta AcAc, bet ne? OHB (Abdelmegeed et al., 2004 ; Shi ir kt., 2014; Shi ir kt., 2016).
Apskritai, dauguma pranešimų sieja OHB su oksidacinio streso susilpnėjimu, nes jo vartojimas slopina ROS / superoksido gamybą, užkerta kelią lipidų peroksidacijai ir baltymų oksidacijai, padidina antioksidacinių baltymų kiekį, pagerina mitochondrijų kvėpavimą ir ATP gamybą (Abdelmegeed et al., 2004; Haces ir kt., 2008; Jain ir kt., 1998; Jain ir kt., 2002; Kanikarla-Marie ir Jainas, 2015; Maaloufas ir kt., 2007; Maaloufas ir Rho, 2008; Marosi ir kt., 2016; Tieu ir kt., 2003; Yin ir kt., 2016; Ziegler ir kt., 2003). Nors AcAc buvo labiau koreliuojamas nei su? OHB su oksidacinio streso indukcija, šis poveikis ne visada lengvai atskiriamas nuo būsimų uždegimą skatinančių reakcijų (Jain ir kt., 2002; Kanikarla-Marie ir Jain, 2015; Kanikarla-Marie ir Jainas, 2016). Be to, labai svarbu atsižvelgti į tai, kad akivaizdi antioksidacinė nauda, kurią suteikia pleiotropinės ketogeninės dietos, negali būti perkelta pačių ketoninių kūnų, o ketoninių kūnų suteikta neuroprotekcija gali būti visiškai nesusijusi su oksidaciniu stresu. Pavyzdžiui, gliukozės trūkumo metu, naudojant žievės neuronų gliukozės trūkumo modelį,? OHB stimuliavo autofaginį srautą ir užkirto kelią autofagosomų kaupimuisi, kuris buvo susijęs su sumažėjusia neuronų mirtimi (Camberos-Luna ir kt., 2016). d-? OHB taip pat indukuoja kanoninius antioksidacinius baltymus FOXO3a, SOD, MnSOD ir katalazę, perspektyviai per HDAC slopinimą (Nagao ir kt., 2016; Shimazu ir kt., 2013).
Nealkoholinių riebalinių liaukų kepenų liga (NAFLD) ir ketonų kūno metabolizmas
Su nutukimu susijęs NAFLD ir nealkoholinis steatohepatitas (NASH) yra dažniausios kepenų ligos priežastys Vakarų šalyse (Rinella ir Sanyal, 2016), o NASH sukeltas kepenų nepakankamumas yra viena iš dažniausių kepenų transplantacijos priežasčių. Nors vien per didelis triacilglicerolių kaupimas hepatocituose,> 5% kepenų svorio (NAFL), nesukelia degeneracinės kepenų funkcijos, žmonėms progresavimas į NAFLD koreliuoja su sisteminiu atsparumu insulinui ir padidėjusia 2 tipo diabeto rizika ir gali prisidėti prie patogenezės. širdies ir kraujagyslių ligos ir lėtinės inkstų ligos (Fabbrini ir kt., 2009; Targher ir kt., 2010; Targher ir Byrne, 2013). NAFLD ir NASH patogeniniai mechanizmai nėra iki galo suprantami, bet apima hepatocitų apykaitos, hepatocitų autofagijos ir endoplazminio tinklelio streso, kepenų imuninių ląstelių funkcijos, riebalinio audinio uždegimo ir sisteminių uždegimo mediatorių anomalijas (Fabbrini ir kt., 2009; Masuoka ir Chalasani, 2013 ; Targher ir kt., 2010; Yang ir kt., 2010). Angliavandenių, lipidų ir aminorūgščių apykaitos sutrikimai pasireiškia nutukime, diabetu ir NAFLD žmonėms ir prisideda prie jų bei modelinių organizmų [apžvelgta (Farese et al., 2012; Lin ir Accili, 2011; Newgard, 2012; Samuel ir 2012). Shulman, 2013; Sun ir Lazar, 2010)]. Nors hepatocitų anomalijos citoplazmos lipidų apykaitoje dažniausiai pastebimos NAFLD (Fabbrini ir kt., 2016b), mitochondrijų metabolizmo, reguliuojančio riebalų oksidacinį šalinimą, vaidmuo NAFLD patogenezėje nėra toks aiškus. Mitochondrijų metabolizmo anomalijos atsiranda ir prisideda prie NAFLD / NASH patogenezės (Hyotylainen et al., 2011; Serviddio et al., 2008; Serviddio et al., 2008; Wei et al., 1974). Yra bendras (Felig ir kt., 2010; Iozzo ir kt., 2015; Koliaki ir kt., 2015; Satapati ir kt., 2012; Satapati ir kt., 2011; Sunny ir kt., 2013), bet nevienodas ( Koliaki ir Roden, 2016; Perry ir kt., 2010; Rector ir kt., 2015) sutaria, kad prieš vystant sąžiningą NASH, kepenų mitochondrijų oksidacija, ypač riebalų oksidacija, padidėja nutukimu, sisteminiu atsparumu insulinui. ir NAFLD. Tikėtina, kad progresuojant NAFLD, atsiranda oksidacinio pajėgumo heterogeniškumas net tarp atskirų mitochondrijų ir galiausiai sutrinka oksidacinė funkcija (Koliaki et al., 2010; Rector et al., 2008; Satapati et al., 2012; Satapati et al. ., XNUMX).
Ketogenezė dažnai naudojama kaip kepenų riebalų oksidacijos atstovas. Ketogenezės pažeidimai atsiranda, kai NAFLD progresuoja gyvūnų modeliuose ir, tikėtina, žmonėms. Per nepilnai apibrėžtus mechanizmus hiperinsulinemija slopina ketogenezę, galbūt prisidedanti prie hipoketonemijos, palyginti su liesa kontrole (Bergman et al., 2007; Bickerton et al., 2008; Satapati et al., 2012; Soeters et al., 2009; Sunny et al. , 2011; Vice ir kt., 2005). Nepaisant to, cirkuliuojančio ketono kūno koncentracijos gebėjimas numatyti NAFLD yra prieštaringas (Mnnist et al., 2015; Sanyal et al., 2001). Patikimi kiekybiniai magnetinio rezonanso spektroskopiniai metodai, naudojant gyvūnų modelius, atskleidė padidėjusį ketonų apykaitos greitį esant vidutiniam atsparumui insulinui, tačiau sumažėjęs rodiklis buvo akivaizdus esant sunkesniam atsparumui insulinui (Satapati ir kt., 2012; Sunny ir kt., 2010). Nutukusių žmonių, kurių kepenys yra riebios, ketogeninis rodiklis yra normalus (Bickerton ir kt., 2008; Sunny ir kt., 2011), todėl ketogenezės rodikliai sumažėja, palyginti su padidėjusiu riebalų rūgščių kiekiu hepatocituose. Vadinasi, a-oksidacijos būdu gautas acetil-CoA gali būti nukreiptas į galutinę oksidaciją TCA cikle, didinant galinę oksidaciją, fosfoenolio piruvato sukeltą gliukoneogenezę per anaplerozę / kataplerozę ir oksidacinį stresą. Acetil-CoA taip pat gali būti eksportuojamas iš mitochondrijų kaip citratas, lipogenezės pirmtako substratas (4 pav.) (Satapati ir kt., 2015; Satapati ir kt., 2012; Solinas ir kt., 2015). Nors ketogenezė tampa mažiau reaguojanti į insuliną ar nevalgius, esant ilgam nutukimui (Satapati ir kt., 2012), pagrindiniai to mechanizmai ir pasekmės vis dar nėra visiškai suprantamos. Naujausi duomenys rodo, kad mTORC1 slopina ketogenezę tokiu būdu, kuris gali būti pasroviui nuo insulino signalizacijos (Kucejova ir kt., 2016), o tai sutampa su pastebėjimais, kad mTORC1 slopina PPARa-tarpinę Hmgcs2 indukciją (Sengupta ir kt., 2010) ( taip pat žr. HMGCS2 ir SCOT / OXCT1 reglamentą).

Preliminarūs mūsų grupės stebėjimai rodo neigiamas ketogeninio nepakankamumo kepenų pasekmes (Cotter ir kt., 2014). Norėdami patikrinti hipotezę, kad sutrikusi ketogenezė, net ir esant daug angliavandenių, taigi ir „ne ketogeninėms“, prisideda prie nenormalaus gliukozės metabolizmo ir sukelia steatohepatitą, mes sukūrėme žymiojo ketogeninio nepakankamumo modelį, skirdami antisense oligonukleotidus (ASO), skirtus Hmgcs2. HMGCS2 praradimas standartinėmis mažai riebalų turinčiomis, karvėmis šeriamomis suaugusiomis pelėmis, sukėlė lengvą hiperglikemiją ir žymiai padidino šimtų kepenų metabolitų gamybą, kurių rinkinys primygtinai siūlė suaktyvinti lipogenezę. Pieno, turinčio nepakankamą ketogenezę, maitinimas labai riebiu maistu sukėlė didžiulį hepatocitų pažeidimą ir uždegimą. Šios išvados patvirtina pagrindines hipotezes, kad (i) ketogenezė nėra pasyvus perpildymo kelias, o dinamiškas mazgas kepenyse ir integruotoje fiziologinėje homeostazėje, ir (ii) atsargus ketogeninis padidėjimas, siekiant sušvelninti NAFLD / NASH, ir sutrikusi gliukozės apykaita kepenyse yra verta tyrinėjimo. .
Kaip sutrikusi ketogenezė gali sukelti kepenų pažeidimą ir pakitusią gliukozės homeostazę? Pirmiausia reikia išsiaiškinti, ar kaltininkas yra ketogeninio srauto trūkumas, ar patys ketonai. Naujausia ataskaita rodo, kad ketonų kūnai gali sušvelninti oksidacinio streso sukeltą kepenų pažeidimą, reaguodami į n-3 polinesočiąsias riebalų rūgštis (Pawlak ir kt., 2015). Primename, kad dėl SCOT ekspresijos trūkumo hepatocituose ketonų kūnai nėra oksiduojami, tačiau jie gali prisidėti prie lipogenezės ir atlikti įvairius signalizavimo vaidmenis, nepriklausomai nuo jų oksidacijos (taip pat žr. Ketoninių kūnų ir? OHB neoksidaciniai metaboliniai likimai signalizuojantis tarpininkas). Taip pat gali būti, kad iš hepatocitų gauti ketonų kūnai gali tarnauti kaip signalas ir (arba) metabolitas gretimiems kepenų tipams, įskaitant žvaigždžių ląsteles ir Kupfferio ląstelių makrofagus. Nors turima ribota literatūra rodo, kad makrofagai negali oksiduoti ketoninių kūnų, tai buvo matuojama tik naudojant klasikines metodikas ir tik pilvaplėvės makrofaguose (Newsholme et al., 1986; Newsholme et al., 1987), o tai rodo, kad vertinimas yra tinkamas, atsižvelgiant į gausią SCOT ekspresiją kaulų čiulpų daromuose makrofaguose (Youm et al., 2015).
Hepatocitų ketogeninis srautas taip pat gali būti citoprotekcinis. Nors išganingi mechanizmai savaime negali priklausyti nuo ketogenezės, mažai angliavandenių turinčios ketogeninės dietos buvo susijusios su NAFLD pagerinimu (Browning ir kt., 2011; Foster ir kt., 2010; Kani ir kt., 2014; Schugaras ir Crawfordas, 2012). . Mūsų pastebėjimai rodo, kad hepatocitų ketogenezė gali grįžti ir reguliuoti TCA ciklo srautą, anaplerozinį srautą, fosfoenolpiruvato daromą gliukoneogenezę (Cotter ir kt., 2014) ir net glikogeno apykaitą. Ketogeninis sutrikimas nukreipia acetil-CoA padidinti TCA srautą, kuris kepenyse buvo susijęs su padidėjusiu ROS sukeltu sužalojimu (Satapati ir kt., 2015; Satapati ir kt., 2012); verčia nukreipti anglį į de novo sintezuojamas lipidų rūšis, kurios gali pasirodyti citotoksinės; ir užkerta kelią NADH reoksidacijai į NAD + (Cotter ir kt., 2014) (4 pav.). Kartu reikia atlikti būsimus eksperimentus, siekiant išspręsti mechanizmus, per kuriuos santykinis ketogeninis nepakankamumas gali tapti netinkamas, prisidėti prie hiperglikemijos, išprovokuoti steatohepatitą ir ar šie mechanizmai veikia žmogaus NAFLD / NASH. Kaip rodo epidemiologiniai duomenys, gali sutrikti ketogenezė progresuojant steatohepatitui (Embade ir kt., 2016; Marinou ir kt., 2011; M. Nistist ir kt., 2015; Pramfalk ir kt., 2015; Safaei ir kt., 2016) terapija, didinanti kepenų ketogenezę, gali būti naudinga (Degirolamo ir kt., 2016; Honda ir kt., 2016).
Ketonų kūnai ir širdies nepakankamumas (HF)
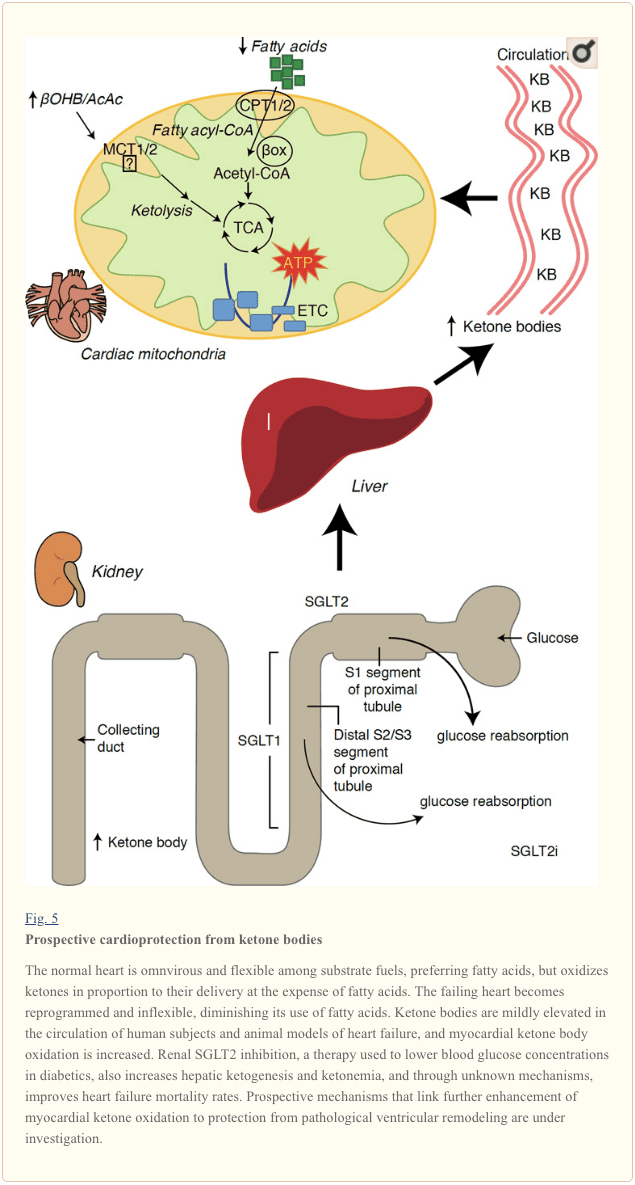
Kai medžiagų apykaitos greitis viršija 400 kcal / kg per parą, o apyvarta yra 6 kg ATP per dieną, širdis yra organas, kuriam tenka didžiausias energijos suvartojimas ir oksidacijos poreikis (Ashrafian ir kt., 35; Wang ir kt., 2007b). Didžioji miokardo energijos apyvartos dalis yra mitochondrijose, o 2010 proc. Šio energijos tiekiama FAO. Širdis normaliomis sąlygomis yra visaėdė ir lanksti, tačiau patologiškai pertvarkoma širdis (pvz., Dėl hipertenzijos ar miokardo infarkto) ir diabetinė širdis tampa metaboliškai nelankstūs (Balasse ir Fery, 70; BING, 1989; Fukao ir kt., 1954 ; Lopaschuk ir kt., 2004; Taegtmeyer ir kt., 2010; Taegtmeyer ir kt., 1980; Young ir kt., 2002). Iš tiesų, genetiškai užprogramuotos širdies degalų apykaitos anomalijos pelių modeliuose išprovokuoja kardiomiopatiją (Carley ir kt., 2002; Neubauer, 2014). Fiziologinėmis sąlygomis normalios širdys oksiduoja ketoninius kūnus proporcingai jų patekimui, riebalų rūgščių ir gliukozės oksidacijos sąskaita, o miokardas yra didžiausias ketonų kūno vartotojas masės vienetui (BING, 2007; Crawford et al., 1954; GARLAND et al. ., 2009; Hasselbaink ir kt., 1962; Jeffrey ir kt., 2003; Pelletier ir kt., 1995; Tardif ir kt., 2007; Yan ir kt., 2001). Palyginti su riebalų rūgščių oksidacija, ketoniniai kūnai yra energetiškai efektyvesni ir duoda daugiau energijos ATP sintezei vienam investuoto deguonies molekulei (P / O santykis) (Kashiwaya ir kt., 2009; Sato ir kt., 2010; Veech, 1995) . Ketono kūno oksidacija taip pat duoda potencialiai didesnę energiją nei FAO, išlaikant oksiduotą ubiquinoną, o tai padidina redokso trukmę elektronų transportavimo grandinėje ir suteikia daugiau energijos ATP sintetinti (Sato ir kt., 2004; Veech, 1995). Ketoninių kūnų oksidacija taip pat gali apriboti ROS gamybą, taigi ir oksidacinį stresą (Veech, 2004).
Preliminarūs intervenciniai ir stebėjimo tyrimai rodo, kad ketoninių organizmų galimas geras poveikis širdžiai. Eksperimentinės išemijos / reperfuzijos žalos kontekste ketonų kūnai suteikė potencialų kardioprotective poveikį (Al-Zaid ir kt., 2007; Wang ir kt., 2008), galbūt dėl padidėjusio mitochondrijų gausumo širdyje arba didelio oksidacinio fosforilinimo tarpininkai (Snorek ir kt., 2012; Zou ir kt., 2002). Naujausi tyrimai rodo, kad pelių (Aubert ir kt., 2016) ir žmonių (Bedi ir kt., 2016) širdies nepakankamumas padidina ketonų kūno panaudojimą, palaikant ankstesnius žmogaus stebėjimus (BING, 1954; Fukao ir kt., 2000; Janardhan ir kt., 2011, Longo ir kt., 2004, Rudolph ir Schinz, 1973, Tildon ir Cornblath, 1972). Širdies nepakankamumu sergantiems pacientams cetokono kūno koncentracijos padidėja tiesiogiai proporcingai užpildymo slėgiui, pastebėjimas, kurio mechanizmas ir svarba lieka nežinomi (Kupari ir kt., 1995, Lommi ir kt., 1996, Lommi ir kt., 1997, Neely ir kt. ., 1972), tačiau pelėms, kurių selektyvus SCOT trūkumas yra kardiomiukai, pasireiškia pagreitintas patologinis skilvelių pertvarkymas ir ROS parašai atsakant į chirurginiu būdu sukeltą slėgio perkrovos sužalojimą (Schugar ir kt., 2014).
Naujausi intriguojantys gydymo cukriniu diabetu stebėjimai parodė galimą ryšį tarp miokardo ketono metabolizmo ir patologinio skilvelių rekonstrukcijos (5 pav.). Inkstų proksimalinių kanalėlių natrio / gliukozės jungtinio transporterio 2 (SGLT2i) slopinimas padidina cirkuliuojančio ketono kūno koncentraciją žmonėms (Ferrannini et al., 2016a, Inagaki ir kt., 2015) ir pelėms (Suzuki ir kt., 2014) padidėjus kepenų ketogenė (Ferrannini ir kt., 2014, Ferrannini ir kt., 2016a, Katz ir Leiter, 2015, Mudaliar ir kt., 2015). Nuostabu, kad bent vienas iš šių agentų sumažino HF hospitalizavimą (pvz., Kaip parodė EMPA-REG tyrimas) ir pagerino mirtingumą nuo širdies ir kraujagyslių sistemos (Fitchett et al., 2016, Sonesson ir kt., 2016, Wu ir kt., 2016a ; Zinman ir kt., 2015). Nors vairuotojų mechanizmai, susiję su naudingais HF rezultatais, susijusiais su SGLT2, lieka aktyviai aptariami, išlikimo nauda greičiausiai bus daugiafaktoriška, perspektyviai apimanti ketozę, bet ir sveikų įtaka svoriui, kraujospūdžiui, gliukozei ir šlapimo rūgšties lygiui, arterijų standumui, simpatinei nervų sistemai, osmotinei diurezės / sumažėjusios plazmos tūrio ir padidėjusio hematokrito (Raz ir Cahn, 2016, Vallon ir Thomson, 2016). Apibendrinant, teigiama, kad teratogeniškai didėjanti ketonemija tiek HF sergantiems pacientams, tiek pacientams, kuriems yra didelė rizika susirgti HF, išlieka prieštaringi, tačiau yra aktyviai tiriama ikiklinikinių ir klinikinių tyrimų metu (Ferrannini ir kt., 2016b; Kolwicz ir kt. 2016; Lopaschuk ir Verma; 2016; Mudaliar ir kt., 2016; Taegtmeyer, 2016).
Ketoninės vėžio biologijos kūnai
Ryšys tarp ketoninių kūnų ir vėžiu sparčiai vystosi, tačiau tyrimai su gyvūnais ir žmonėmis leidžia daryti įvairias išvadas. Kadangi ketonų metabolizmas yra dinamiškas ir jautriai reaguojantis į maistinę būklę, jis vilioja siekti biologinių ryšių su vėžiu, nes gali būti tiksliai reguliuojamos mitybos terapijos. Vėžio ląstelės patiria metabolinį perprogramavimą, kad išlaikytų greitą ląstelių proliferaciją ir augimą (DeNicola ir Cantley, 2015, Pavlova ir Thompson, 2016). Klasikinis Warburg poveikis vėžio ląstelių metabolizmui atsiranda dėl vyraujančio glikolizės ir pieno rūgšties fermentacijos vaidmens perkeliant energiją ir kompensuojant mažesnę priklausomybę nuo oksidacinio fosforilinimo ir riboto mitochondrinio kvėpavimo (De Feyter ir kt., 2016; Grabacka et al., 2016; Kang ir kt., 2015; Poff ir kt., 2014; Shukla ir kt., 2014). Gliukozės anglis pirmiausia yra nukreiptas per glikolizę, pentozės fosfato kelią ir lipogenezę, kurie kartu suteikia tarpinių junginių, reikalingų navikų biomasės plitimui (Grabacka ir kt., 2016, Shukla ir kt., 2014, Yoshii ir kt., 2015). Vėžio ląstelių pritaikymas prie gliukozės nepakankamumo atsiranda dėl galimybės naudoti alternatyvius degalų šaltinius, įskaitant acetatą, glutamatą ir aspartatą (Jaworski ir kt., 2016, Sullivan ir kt., 2015). Pavyzdžiui, ribota prieiga prie piruvato atskleidžia vėžio ląstelių galimybę glutaminu konvertuoti į acetil-CoA karboksilinant, išlaikant tiek energetinius, tiek anabolinius poreikius (Yang ir kt., 2014). Įdomus vėžio ląstelių pritaikymas yra acetato panaudojimas kaip kuras (Comerford ir kt., 2014, Jaworski ir kt., 2016, Mashimo ir kt., 2014, Wright ir Simone, 2016, Yoshii ir kt., 2015). Acetatas taip pat yra lipogenezės pagrindas, kuris yra svarbus naviko ląstelių proliferacijai, o šio lipogeninio kanalo padidėjimas yra susijęs su trumpesniu išgyvenimu pacientams ir didesne naviko našta (Comerford ir kt., 2014; Mashimo ir kt., 2014; Yoshii et al. ., 2015).
Nevėžinės ląstelės gliukozės trūkumo metu lengvai perkelia savo energijos šaltinį iš gliukozės į ketoninius kūnus. Šis plastiškumas gali būti įvairesnis tarp vėžinių ląstelių tipų, tačiau in vivo implantuoti smegenų augliai oksiduojasi [2,4-13C2] -? OHB panašiu laipsniu kaip ir aplinkiniai smegenų audiniai (De Feyter et al., 2016). „Atvirkštinio Warburgo efekto“ arba „dviejų skyrių naviko metabolizmo“ modeliai kelia prielaidą, kad vėžinės ląstelės skatina OHB gamybą gretimuose fibroblastuose, tenkindamos naviko ląstelių energijos poreikius (Bonuccelli ir kt., 2010; Martinez-Outschoorn ir kt., 2012). . Kepenyse hepatocitų perėjimas nuo ketogenezės prie ketonų oksidacijos hepatoceliulinės karcinomos (hepatomos) ląstelėse atitinka BDH1 ir SCOT aktyvacijos aktyvumą, pastebėtą dviejose hepatomos ląstelių linijose (Zhang et al., 1989). Iš tiesų, hepatomos ląstelės ekspresuoja OXCT1 ir BDH1 ir oksiduoja ketonus, tačiau tik tada, kai serumas badauja (Huang ir kt., 2016). Taip pat buvo pasiūlyta naviko ląstelių ketogenezė. Dinamiški ketogeninių genų ekspresijos pokyčiai pasireiškia vėžio metu virstant gaubtinės žarnos epiteliui, ląstelių tipui, kuris paprastai išreiškia HMGCS2, o naujausioje ataskaitoje teigiama, kad HMGCS2 gali būti blogos kolorektalinių ir plokščiųjų ląstelių karcinomų prognozės žymeklis (Camarero ir kt., 2006; Chen ir kt., 2016). Ar šiai asociacijai reikalinga ketogenezė, ar HMGCS2 mėnulio apšvietimo funkcija, dar reikia nustatyti. Ir atvirkščiai, akivaizdi melanomos ir glioblastomos ląstelių OHB gamyba, kurią stimuliuoja PPAR? agonistas fenofibratas, buvo susijęs su augimo sustabdymu (Grabacka ir kt., 2016). Norint apibūdinti HMGCS2 / SCOT ekspresijos, ketogenezės ir ketonų oksidacijos vėžinėse ląstelėse vaidmenis, reikalingi tolesni tyrimai.
Be degalų apykaitos srities, ketonai neseniai buvo įtraukti į vėžio ląstelių biologiją per signalizacijos mechanizmą. BRAF-V600E + melanomos analizė parodė nuo OCT1 priklausomą HMGCL indukciją onkogeniniu BRAF priklausomu būdu (Kang ir kt., 2015). HMGCL padidėjimas buvo susijęs su didesne ląstelių AcAc koncentracija, o tai savo ruožtu sustiprino BRAFV600E-MEK1 sąveiką, sustiprindama MEK-ERK signalizaciją perdavimo grandinėje, kuri skatina naviko ląstelių proliferaciją ir augimą. Šie pastebėjimai kelia intriguojantį perspektyvios ekstrahepatinės ketogenezės klausimą, kuris tada palaiko signalizacijos mechanizmą (taip pat žr.? OHB kaip signalizavimo tarpininką ir prieštaravimus ekstepepatinėje ketogenezėje). Taip pat svarbu atsižvelgti į nepriklausomą AcAc, d-OHB ir XNUMX-OHB poveikį vėžio metabolizmui, o svarstant HMGCL, leucino katabolizmas taip pat gali būti sutrikęs.
Ketogeninių dietų (taip pat žr. Ketogeninės dietos ir egzogeninių ketoninių kūnų terapinis naudojimas) poveikis vėžio gyvūnų modeliams yra įvairus (De Feyter et al., 2016; Klement et al., 2016; Meidenbauer et al., 2015; Poff et al.) ., 2014; Seyfried ir kt., 2011; Shukla ir kt., 2014). Nors diskutuojama apie nutukimo, vėžio ir ketogeninės dietos epidemiologines sąsajas (Liskiewicz ir kt., 2016; Wright ir Simone, 2016), metaanalizė, kurioje gyvūnų modeliuose ir žmogaus tyrimuose buvo naudojamos ketogeninės dietos, pasiūlė teigiamą poveikį išgyvenimui. nauda, perspektyviai susijusi su ketozės dydžiu, dietos pradžios laiku ir naviko vieta (Klement et al., 2016; Woolf et al., 2016). Kasos vėžio ląstelių gydymas ketonų kūnais (d-? OHB arba AcAc) slopino augimą, proliferaciją ir glikolizę, o ketogeninė dieta (81% kcal riebalų, 18% baltymų, 1% angliavandenių) in vivo sumažino naviko svorį, glikemiją ir padidėjęs gyvūnų, kuriems yra implantuotas vėžys, raumenų ir kūno svoris (Shukla ir kt., 2014). Panašūs rezultatai buvo pastebėti naudojant metastazavusį glioblastomos ląstelių modelį pelėms, kurioms dieta buvo skirta papildyti ketonais (Poff ir kt., 2014). Priešingai, ketogeninė dieta (91% kcal riebalų, 9% baltymų) padidino cirkuliuojančios? OHB koncentraciją ir sumažino glikemiją, tačiau neturėjo jokios įtakos nei naviko kiekiui, nei gliomą turinčių žiurkių išgyvenamumui (De Feyter et al., 2016). Gliukozės ketonų indeksas buvo pasiūlytas kaip klinikinis rodiklis, kuris pagerina metabolinį ketogeninės dietos sukeltos smegenų vėžio terapijos valdymą žmonėms ir pelėms (Meidenbauer et al., 2015). Kartu ketoninių medžiagų apykaitos ir ketoninių kūnų vaidmuo vėžio biologijoje yra viliojantis, nes kiekvienas iš jų kelia terapines galimybes, tačiau pagrindiniai aspektai vis dar turi būti išaiškinti, o kintamųjų matricoje atsiranda aiški įtaka, įskaitant i) egzogeninio ketono skirtumus. kūnai, palyginti su ketogenine dieta, ii) vėžio ląstelių tipas, genominiai polimorfizmai, laipsnis ir stadija; ir iii) ketotinės būsenos poveikio laikas ir trukmė.

Ketogenezę sukūrė ketoniniai kūnai per riebalų rūgščių ir ketogeninių amino rūgščių skilimą. Šis biocheminis procesas suteikia energijos įvairiems organams, ypač smegenims, valgymo metu, nes atsakas į gliukozės koncentraciją kraujyje yra nepasiekiamas. Ketonai daugiausia gaminami kepenų ląstelių mitochondrijose. Nors kitos ląstelės gali atlikti ketogenezę, jos nėra tokios veiksmingos, kaip kepenų ląstelės. Kadangi mitochondrijų atsiranda ketogenezė, jos procesai yra reguliuojami nepriklausomai. Dr Alex Jimenez DC, CCST Insight
Terapinis ketogeninės dietos ir egzogeninių ketoninių kūnų panaudojimas
Ketogeninių dietų ir ketoninių kūnų, kaip terapinių priemonių, taikymas atsirado ir nevėžiniuose kontekstuose, įskaitant nutukimą ir NAFLD / NASH (Browning ir kt., 2011; Foster ir kt., 2010; Schugaras ir Crawfordas, 2012); širdies nepakankamumas (Huynh, 2016; Kolwicz et al., 2016; Taegtmeyer, 2016); neurologinė ir neurodegeneracinė liga (Martin ir kt., 2016; McNally ir Hartman, 2012; Rho, 2015; Rogawski ir kt., 2016; Yang ir Cheng, 2010; Yao ir kt., 2011); įgimtos medžiagų apykaitos klaidos (Scholl-B rgi ir kt., 2015); ir pratimų atlikimas (Cox et al., 2016). Ketogeninių dietų veiksmingumas ypač vertinamas gydant epilepsijos priepuolius, ypač pacientams, atspariems vaistams. Daugumoje tyrimų buvo įvertinta ketogeninė dieta vaikams ir nustatyta, kad po 50 mėnesių priepuolių dažnis sumažėja iki ~ 3%, o pasirinktų sindromų efektyvumas yra didesnis (Wu ir kt., 2016b). Patirtis yra ribotesnė suaugusiųjų epilepsijos atveju, tačiau akivaizdus panašus sumažėjimas, geresnis atsakas simptominės generalizuotos epilepsijos pacientams (Nei ir kt., 2014). Pagrindiniai antikonvulsiniai mechanizmai lieka neaiškūs, nors teigiamos hipotezės yra sumažėjęs gliukozės panaudojimas / glikolizė, perprogramuotas glutamato transportas, netiesioginis poveikis ATP jautriam kalio kanalui ar adenozino A1 receptoriams, natrio kanalo izoforminės išraiškos pasikeitimas arba poveikis cirkuliuojantiems hormonams, įskaitant leptiną ( Lambrechts ir kt., 2016; Lin ir kt., 2017; Lutas ir Yellen, 2013). Lieka neaišku, ar prieštraukulinis poveikis visų pirma yra susijęs su ketono kūnais, ar dėl kaskadinių metabolinių pasekmių, susijusių su mažai angliavandenių turinčiomis dietomis. Nepaisant to, ketonų esteriai (žr. Toliau), atrodo, padidina priepuolių slenkstį išprovokuotų priepuolių gyvūnų modeliuose (Ciarlone ir kt., 2016; D'Agostino ir kt., 2013; Viggiano ir kt., 2015).
Atkinso ir ketogeninės dietos su mažai angliavandenių dažnai laikomos nemaloniais ir gali sukelti vidurių užkietėjimą, hiperurikemiją, hipokalcemiją, hipomagnezemiją, sukelti nefrolitiazę, ketoacidozę, sukelti hiperglikemiją, didinti cirkuliuojančio cholesterolio ir laisvųjų riebalų rūgščių koncentraciją (Bisschop ir kt., 2001 , Kossoff ir Hartman, 2012, Kwiterovich ir kt., 2003, Suzuki ir kt., 2002). Dėl šių priežasčių ilgalaikis laikymasis kelia problemų. Graužikų tyrimuose dažniausiai naudojamas išskirtinis makroelementų pasiskirstymas (94% kcal riebalų, 1% kcal angliavandenių, 5% kcal baltymų, Bio-Serv F3666), kuris sukelia stiprų ketozę. Tačiau baltymų kiekio padidėjimas net 10% kcal žymiai sumažina ketozę, o 5% kcal baltymų apriboja metabolinius ir fiziologinius padarinius. Ši dieta taip pat yra cholino išeikvota, kitas kintamasis, turintis įtakos jautrumui kepenų pažeidimui ir net ketogenezei (Garbow ir kt., 2011; Jornayvaz ir kt., 2010; Kennedy ir kt., 2007; Pissios ir kt., 2013; Schugar et al., 2013). Ilgalaikio ketogeninio mitybinio vartojimo pelėms poveikis dar nėra išsamiai apibrėžtas, tačiau naujausi pelių tyrimai parodė, kad pelėms būdingas įprastas išgyvenimas ir ketogeninės dietos piktybinės žaizdos piktogramos per visą jų gyvenimo trukmę, nors aminorūgščių metabolizmas, energijos sąnaudos ir insulino signalai buvo žymiai perprogramuotos (Douris et al., 2015).
Mechanizmai, didinantys ketozę, naudojant alternatyvius ketogeninių mitybos būdus, apima pernešamų ketono kūno pirmtakų naudojimą. Eksogeninių ketoninių kūnų administravimas gali sukurti unikalią fiziologinę būklę, kuri nebūdinga įprastoje fiziologijoje, nes cirkuliuojanti gliukozė ir insulino koncentracija yra santykinai normalios, o ląstelės gali užkirsti kelią gliukozės įsisavinimui ir utilizavimui. Pačių ketoninių kūnų pusinės eliminacijos laikas yra trumpas, o nurijus ar užpylus natrio? OHB druskos, kad būtų pasiekta terapinė ketozė, išprovokuojama nenormali natrio apkrova. R / S-1,3-butandioolis yra netoksiškas dialkoholis, kuris lengvai oksiduojamas kepenyse, gaunant d / 1992-OHOH (Desrochers ir kt., XNUMX). Skirtinguose eksperimentiniuose kontekstuose ši dozė pelėms ar žiurkėms buvo vartojama kasdien net septynias savaites, per 5 valandas po vartojimo cirkuliuojančios a OHB koncentracijos buvo iki 2 mM, o tai yra stabili mažiausiai dar 3 valandas (D ' Agostino ir kt., 2013). Graužikams, kuriems buvo suteiktas R / S-1,3-butanediolis (Carpenter ir Grossman, 1983), buvo pastebėtas dalinis maisto vartojimo slopinimas. Be to, trys chemiškai skirtingi ketonų esteriai (KE), (i) R-1,3-butandiolio monoesteris ir d-OHOH (R-3-hidroksibutilas R-OHB); (ii) gliceril-tris-a-OHB; ir (iii) taip pat buvo plačiai ištirtas R, S-1,3-butandiolio acetoacetato diesteris (Brunengraber, 1997; Clarke ir kt., 2012a; Clarke ir kt., 2012b; Desrochers ir kt., 1995a; Desrochers ir kt. ., 1995b; Kashiwaya ir kt., 2010). Būdingas pirmojo pranašumas yra tai, kad po esterazės hidrolizės žarnyne ar kepenyse susidaro 2 moliai fiziologinio d-? OHB vienam moliui KE. Saugumas, farmakokinetika ir tolerancija buvo plačiausiai ištirti žmonėms, vartojantiems R-3-hidroksibutil-R-OHB dozes iki 714 mg / kg, o cirkuliuojančios d-OHHB koncentracijos buvo iki 6 mM (Clarke ir kt., 2012a; Cox ir kt., 2016; Kemper ir kt., 2015; Shivva ir kt., 2016). Graužikuose ši KE sumažina kalorijų vartojimą ir plazmos bendrą cholesterolį, stimuliuoja rudąjį riebalinį audinį ir pagerina atsparumą insulinui (Kashiwaya ir kt., 2010, Kemper ir kt., 2015, Veech, 2013). Naujausi duomenys rodo, kad treniruojantis sportuojantiems žmonėms, vartojant R-3-hidroksibutilą R-OHB, sumažėjo griaučių raumenų glikolizė ir laktato koncentracija plazmoje, padidėjo triacilglicerolio raumenis oksiduojantis raumenys ir išliko raumenų glikogeno kiekis, net jei kartu vartojami angliavandeniai stimuliavo insulino sekreciją ( Cox ir kt., 2016). Būtina tolesnė šių intriguojančių rezultatų plėtra, nes ištvermės pratimų efektyvumą daugiausia lėmė griežtas atsakas į KE 2 / 8 subjektus. Nepaisant to, šie rezultatai remia klasikinius tyrimus, kurie rodo ketonų oksidacijos pirmenybę kituose substratuose (GARLAND ir kt., 1962; Hasselbaink ir kt., 2003; Stanley ir kt., 2003; Valente-Silva ir kt., 2015); įskaitant treniruotes, ir kad apmokyti sportininkai gali būti labiau gruntuojami, kad galėtų naudoti ketonus (Johnson ir kt., 1969a, Johnson ir Walton, 1972, Winder ir kt., 1974, Winder ir kt., 1975). Galiausiai, turi būti nustatyti mechanizmai, kurie galėtų palaikyti geresnį pratimų skaičių, kai vienodo kalorijų kiekio (skiriamo makroelementų) ir vienodo deguonies suvartojimo lygis.
Ateities perspektyvos
Naujausi stebėjimai, iš esmės stigmatizuoti kaip perpildymo kelias, galintys kaupti toksiškas emisijas iš riebalų deginimo ribotose angliavandenių būsenose („ketotoksinio paradigma“), ketonų kūno apykaita tarnauja išganingiems vaidmenims net ir esant angliavandenių turinčioms būsenoms, atverdama „ketohormetinę“ Hipotezė. Nors lengvas mitybos ir farmakologinis požiūris į manipuliavimą ketonų metabolizmu paverčia jį patraukliu terapiniu taikiniu, agresyviai keliami, tačiau apdairūs eksperimentai išlieka tiek pagrindinių, tiek vertimo tyrimų laboratorijose. Nepatenkinti poreikiai atsirado apibrėžiant ketonų metabolizmo skatinimo vaidmenį širdies nepakankamumo, nutukimo, NAFLD / NASH, 2 tipo diabeto ir vėžio srityse. Ketoninių kūnų „nekanoninio“ signalizavimo vaidmens apimtis ir poveikis, įskaitant PTM reguliavimą, kurie greičiausiai grįžta atgal į metabolizmo ir signalizacijos kelius, reikalauja giliau tyrinėti. Galiausiai, ekstrahepatinė ketogenezė gali atverti intriguojančius parakrino ir autokrininio signalo perdavimo mechanizmus ir galimybes paveikti bendrą metabolizmą nervų sistemoje ir navikuose, kad būtų pasiekti terapiniai tikslai.
Padėka
Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/
Išnašos
Apibendrinant galima pasakyti, kad ketono kūnus sukuria kepenys, kad būtų galima naudoti kaip energijos šaltinį, kai žmogaus organizme nėra pakankamai gliukozės. Ketogenezė atsiranda, kai kraujyje yra mažas gliukozės kiekis, ypač po to, kai išnaudojamos kitos ląstelių angliavandenių atsargos. Ankstesnio straipsnio tikslas buvo aptarti daugialypius ketoninių kūnų vaidmenis kuro apykaitoje, signalizacijoje ir terapijoje. Mūsų informacijos apimtis apsiriboja chiropraktikos ir stuburo sveikatos problemomis. Norėdami aptarti temą, nedvejodami kreipkitės į daktarą Jimenezą arba susisiekite su mumis adresu915-850-0900.
Kuratorius dr. Alexas Jimenezas
Nurodoma iš: Ncbi.nlm.nih.gov/pmc/articles/PMC5313038/

Papildoma temos diskusija: ūmus nugaros skausmas
Nugaros skausmasYra viena iš labiausiai paplitusių neįgalumo priežasčių ir praleistų dienų darbe visame pasaulyje. Nugaros skausmai priskiriami antra pagal dažnumą gydytojų kabinetų apsilankymų priežastims, kurių yra tik viršutinių kvėpavimo takų infekcijos. Maždaug 80 procentų gyventojų bent kartą gyvenime patirs nugaros skausmus. Stuburas yra sudėtinga struktūra, kurią sudaro kaulai, sąnariai, raiščiai ir raumenys, be kitų minkštųjų audinių. Traumos ir (arba) sunkinančios sąlygos, pvz.,herniuotieji diskai, ilgainiui gali sukelti nugaros skausmo simptomus. Sporto traumos ar automobilio avarijos dažnai yra dažniausia nugaros skausmo priežastis, tačiau kartais paprasčiausi judesiai gali sukelti skaudžius rezultatus. Laimei, alternatyvios gydymo galimybės, tokios kaip chiropraktikos priežiūra, gali padėti sumažinti nugaros skausmą, naudojant stuburo koregavimą ir rankines manipuliacijas, galiausiai pagerinant skausmo malšinimą.

EXTRA EXTRA | SVARBIAMA TEMA: Rekomenduojama El Paso, TX Chiropractor
***